-
脓毒血症是指机体受到重大烧伤、创伤、严重感染后引起的剧烈的全身炎症反应,病程发展快,可引起发热、血压急剧下降等临床表现,随着病程进展,会造成肺、肝、心等脏器的进一步损伤,甚至导致病人因多器官功能障碍而死亡。在我国医院ICU中脓毒血症的发病率为28.7%,而病死率为33.5%[1],在美国每年因脓毒血症住院的病人病死率高达14%~29%[2]。在澳大利亚和新西兰入住ICU的病人脓毒血症发病率为7%~11%,同时医院病死率为18%~35%[3]。近年来,随着耐药菌株的逐年增多,治疗手段的局限性,脓毒血症的病死率居高不下。脓毒血症基础研究进展缓慢,与动物模型不稳定、无法很好模拟脓毒血症临床病理生理变化密切相关。研究[4]表明,肺脏结构及功能的病理生理学改变可以反映原始损伤与病理机制之间的动态平衡,急性肺损伤是脓毒血症的一个重要表现。肺损伤是脓毒血症病人死亡的主要原因,与脓毒血症的预后密切相关。本文就盲肠结扎穿刺建造的脓毒血症小鼠模型中肺组织损伤的相关机制作一探讨。
-
选用42只C57/BL6小鼠,均购于上海杰思捷实验动物有限公司,为6周龄健康雄鼠,体质量(22.3±1.9)g。实验生产许可证:SCXK(沪)2013-0006。动物实验均遵从上海交通大学附属第九人民医院动物伦理条例。将实验用小鼠于SPF级动物房标准喂养4周。
-
戊巴比妥钠(天津金耀氨基酸有限公司),4%多聚甲醛(上海实验试剂有限公司),苏木素-伊红染液(武汉谷歌生物科技有限公司),实时荧光定量-聚合酶链反应(RT-PCR)逆转录试剂盒和荧光染料(美国天根公司),PCR引物合成(上海生工生物工程股份有限公司),EDTA抗原修复液(美国Servicebio公司);Light Cycler 480荧光定量PCR仪(瑞士Roche公司),5810R Centrifuge高速低温水平离心机(德国Eppendorf公司), NIKON ECLIPSE CI正置光学显微镜及NIKON DS-U3成像系统(日本NIKAON公司)。
-
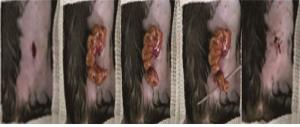
42只C57BL/6小鼠随机分为正常对照组、假手术组、脓毒血症组,每组14只。脓毒血症组小鼠处理(见图 1):手术前6 h禁食水,按照戊巴比妥钠35~45 mg/kg腹腔麻醉后,脱毛膏去除左下腹毛发,暴露手术区;消毒铺巾,定位左肋弓下1~1.5 cm,腹中线左外侧0.3~0.4 cm,用手术刀切开0.5 cm纵行切口,依次切开皮肤、皮下结缔组织、腹部肌层、腹膜,于左后下方寻找盲肠并暴露。以5号编织线在距回盲瓣至盲肠尖近端1/3处结扎盲肠,用5 mL注射器针头在结扎部位远端十字对穿盲肠,挤出少量粪便置于腹腔内。回纳盲肠,逐层缝合关闭腹腔。手术过程几乎无出血,皮下注射0.1 mL 0.9%氯化钠注射液用于术后补液。手术全程保暖,术后正常饲养。假手术组不进行十字对穿盲肠,直接回纳腹腔,其余处理步骤同脓毒血症组。
-
术前、术后所有小鼠空腹称量体质量,术前15 min麻醉,于处理后24 h眼球取血,取血后颈椎脱位法处死小鼠,即刻取出全肺组织,一部分使用4%多聚甲醛固定,石蜡包埋切片,另一部分肺组织液氮保存,用以检测肿瘤坏死因子α(TNF-α)和白细胞介素(IL)-6水平。
-
参照文献[5],评分包括外观、意识水平、活动度、刺激反应、眼部情况、呼吸速率、呼吸质量7个指标,每个指标按照等级为0~4分,评分为7个指标分数相加。
-
验证脓毒血症小鼠的生存率,将相同周龄、雄性的正常小鼠、假手术小鼠和脓毒血症小鼠各8只,手术成功后麻醉苏醒分笼放回动物房饲养,正常饮食,每8 h观察1次,记录其生存与死亡,直至脓毒血症小鼠全部死亡结束观察。
-
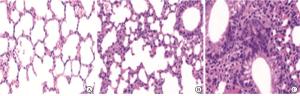
肺组织形态观察:将固定于4%多聚甲醛24 h的新鲜组织于脱水机内依次梯度乙醇脱水,将浸好腊的组织放入包埋机内包埋,蜡块在切片机切片4 μm厚度,40 ℃温水中展平,载玻片捞起,60 ℃烤箱内烤片,常温备用。将石蜡切片依次放入二甲苯、乙醇脱蜡至水:入Harris苏木素染3~8 min,水洗,1%盐酸分化数秒,0.6%氨水返蓝:入伊红染色液中染色1~3 min:依次于乙醇、二甲苯中脱水透明,中性树脂封片,显微镜下镜检,其中细胞核呈蓝色,细胞质呈红色。观察肺组织中渗出、渗血、碎片及炎症浸润情况。
-
以HE染色组织切片为参照依据,分别以渗出物情况、充血程度、肺泡内出血和组织碎片、中性粒细胞浸润、细胞病理性增生等5项病理指标进行评分。其中无、轻度、中度、重度分别计分0、1、2、3分。5项分值相加,总分即为肺组织损伤评分。
-
MPO免疫荧光检测:将石蜡切片依次放入二甲苯、乙醇脱蜡至水,使用EDTA抗原修复缓冲液(pH8.0)将组织切片进行抗原修复,切片稍甩干后用组化笔在组织周围画圈荧光淬灭,圈内滴加牛血清白蛋白行血清封闭,在切片上滴加一抗(MPO 1: 200稀释),孵育过夜,玻片脱色洗涤后,将切片稍甩干后在圈内滴加与二抗(Alexa 488-山羊抗兔IgG 1: 400稀释)覆盖组织,避光孵育,DAPI复染细胞核,使用抗荧光淬灭封片剂封片,切片于荧光显微镜下观察并采集图像。其中DAPI染色的细胞核在紫外的激发下为蓝色,MPO阳性表达细胞为相应荧光素标记的绿色。
-
采用RT-PCR方法,逆转录和荧光染料由美国天根公司生产。取1 cm2大小组织,反复使用液氮研磨至粉末状,Trizol消化、裂解组织后使用氯仿溶解RNA,取上层水相,分别使用异丙醇、75%乙醇沉淀、清洗RNA,沉淀RNA使用DEPC H2O,在55~60 ℃溶解,测定RNA浓度。使用快速反转录试剂盒中5×gDNA Buffer、FQ-RT Primer Mix、10×Fast RT Buffer、RNase-Free ddH2O试剂合成第一链cDNA。整个过程避免外界RNA酶降解RNA,合成的cDNA可用于后续实验或者低温保存。使用荧光染料QuantiNovaTM SYRB Green PCR Kit、前期合成的cDNA、TNF-α引物(Forward 5′-CCC TCA CAC TCA GAT VAT CTT CT-3′; Reverse 5′-GCT ACG ACG TGG GCT ACA G-3′)、IL-6引物(Forward 5′-GCA ACT GTT CCT GAA CTC AAC T-3′; Reverse 5′-ATC TTT TGG GGT CCG TCA ACT-3′)按比例加入96孔板,扩增。
-
采用t检验、方差分析、q检验和Kaplan-Meier法生存分析。
-
脓毒血症组小鼠脓毒血症情况评分较正常对照组、假手术明显升高(P<0.01),而假手术组脓毒血症情况评分较正常对照组明显升高(P<0.01)(见表 1)。正常对照组肺泡结构完整、清晰,肺间隔内无水肿,肺组织内无细胞碎片、充血、渗出,无炎性细胞浸润。假手术组肺损伤较轻,肺泡形态结构较完整,肺间隔轻微水肿、增厚,清晰可见并且连续,肺泡内细胞碎片、充血、渗出较少,肺炎症浸润较轻。脓毒血症组小鼠肺损伤重,肺泡结构破坏严重,形态结构不清晰,间隔水肿严重,肺泡内渗出、充血及各种细胞碎片较多,炎症细胞浸润多。假手术组肺组织考虑到小鼠全身麻醉、腹部创伤,因此也会出现轻微肺损伤(见图 2)。肺组织损伤评分差异有统计学意义(P<0.01)(见表 1),MPO免疫荧光显示肺组织浸润的炎性细胞主要为中性粒细胞(见图 3),脓毒血症组的炎性细胞较正常对照组、假手术组都有明显的增加(P<0.01)(见表 1),术后24 h脓毒血症组小鼠的肺组织中的TNF-α及IL-6水平均较正常对照组、假手术组明显升高(P<0.01)(见表 1)。
分组 n MSS 肺组织损伤评分 炎性细胞 TNF-α IL-6 正常对照组 14 — 0.67±0.21 1 080±188.0 1.000±0.000 1.000±0.000 假手术组 14 4.14±0.27** 3.50±0.22** 2 699±285.6** 2.070±0.383* 1.578±0.084** 脓毒血症组 14 20.50±0.68**△△ 11.00±0.45**△△ 16 948±401.9**△△ 9.300±1.107**△△ 451.000±36.760**△△ F — 659.90 290.49 686.50 44.53 149.70 P — <0.01 <0.01 <0.01 <0.01 <0.01 MS组内 — 1 645.000 0.098 1.906×108 120.300 404 414.000 q检验:与正常对照组比较*P<0.05;**P<0.01,与假手术组比较△△P<0.01 表 1 3组相关指标比较(x±s)
-
正常对照组小鼠、假手术组小鼠观察期间无小鼠死亡。而脓毒血症组小鼠16 h即出现第1例死亡,术后24 h脓毒血症组小鼠生存率为75.0%,而术后32 h小鼠生存率仅为37.5%,术后40 h小鼠生存率维持在25.0%,直至术后96 h,脓毒血症小鼠全部死亡。脓毒血症组小鼠32 h(χ2=12.62,P<0.01)、48 h(χ2=14.83,P<0.01)生存率较正常对照组、假手术组明显降低。
-
脓毒血症是一种常见的严重的全身性感染,具有病死率高、治疗费用高昂等特点。已知的脓毒血症治疗措施,如使用内毒素拮抗剂、分子靶向治疗、使用镇静药等,由于疗效欠佳,均无法达到共识[6-9]。受多种条件的限制,脓毒血症的临床研究进展缓慢,有学者[10-13]致力于脓毒血症的基础研究。近年来,脓毒血症的基础研究发展迅速,已取得一定成果。动物模型是研究疾病的致病机制、病理生理过程以及药物研发的重要工具,在基础研究中占据关键地位。从血清学检查、临床症状、发病因素、疾病发生发展等方面模拟脓毒血症的多种动物模型的成功建立,解决了因脓毒血症进展快、病理病生变化复杂多样,在使用动物模型模拟脓毒血症临床病理变化和特征较为困难的问题。从生物学行为、实验室检查、分子生物学、信号转导等环节提供了大量的实验数据[14-15]。本实验选用的盲肠结扎穿刺(CLP)模型通过穿刺引起肠道内菌丛诱发腹膜炎,经过不断改进,与临床脓毒血症最为接近,主要体现在血液动力学及免疫状态变化等方面,且病情非一过性,而是处在不断变化中,能较好地模拟脓毒血症的变化过程。并且,CLP模型小鼠从手术到死亡仅经历数天,为研究者提供了较充足的研究时间,是脓毒血症动物模型的“金标准”[16]。
机体发生脓毒血症后,产生的大量前炎症介质及脂质代谢产物,促进了炎症细胞(尤其是中性粒细胞)在肺组织的聚集和活化,构成了急性肺损伤炎性反应的“瀑布样”放大效应,随着炎症的进一步发展,导致肺泡间隙水肿、肺泡的塌陷及透明膜的形成,造成肺泡的不可逆损伤,导致了肺顺应性的降低,增加了肺泡死腔,病人发生顽固的低氧血症,进而造成机体的死亡。临床上,超过50%的脓毒血症病患会发展为急性肺损伤(ALI) /急性呼吸窘迫综合征(ARDS) [17]。本研究发现,与CLP模型组比较,正常对照组小鼠肺组织病理表现为肺泡的结构完整,无炎性细胞浸润,肺泡间隔正常。CLP组小鼠发生继发性肺损伤,表现为肺泡腔和肺泡间隔有大量炎症细胞(免疫荧光证实CLP模型组的炎性浸润细胞为中性粒细胞)、碎片和红细胞浸润,肺泡结构破坏,肺泡间隔明显水肿、增厚。表明CLP诱导的脓毒血症模型被成功复制,且诱发了肺损伤。与ALI/ARDS的肺组织病理学改变如肺泡结构被破坏、中性粒细胞浸润、肺泡腔充血以及透明膜的形成等极为相似。而在肺损伤中中性粒细胞通过与上皮细胞和内皮细胞发生黏附作用,进一步加重肺部损伤[18]。有研究[19-20]证实TNF-α是脓毒血症时最早释放的因子之一,是炎症反应中激活细胞因子级联反应的主要炎性介质;而IL-6水平的高低与疾病严重程度及预后相关。与正常对照组比较,CLP模型组中小鼠肺组织中TNF-α、IL-6水平均明显升高。
由此,我们推测肺组织的变化是由于脓毒血症中肺组织中大量的中性细胞的聚集和活化,通过黏附作用进一步破坏肺部上皮和血管内皮,致肺组织损伤无法逆转造成的,这一肺损伤导致ALI/ARDS的发生,提高了脓毒血症的死亡率。同时肺组织中TNF-α和IL-6水平明显升高,进一步加重脓毒血症所致急性肺损伤的严重程度。提示CLP小鼠致脓毒血症可造成肺组织严重损伤。需要指出的是,本次研究样本量有限,监测与肺损伤有关指标的特异性及敏感性有待进一步验证,尚需开展更多的基础及临床试验进行更深入的研究。
脓毒血症小鼠致肺损伤模型的研究
Study on the model of lung injury induced by sepsis in mice
-
摘要:
目的探讨盲肠结扎穿刺建造的脓毒血症小鼠模型中肺组织损伤的相关机制。 方法选取42只C57BL/6雄性小鼠,随机分为正常对照组、假手术组及脓毒血症组,各14只。正常对照组不做处理,假手术组行盲肠结扎,脓毒血症组予以盲肠结扎穿刺。24 h收集各组肺组织,观察脓毒血症情况评分(MSS)、生存率、肺组织形态改变情况、肺组织损伤评分、中性粒细胞以及肺组织中炎症因子肿瘤坏死因子α(TNF-α)和白细胞介素(IL)-6表达水平的差异。 结果脓毒血症组MSS评分、肺损伤评分、中性粒细胞数、TNF-α及IL-6表达水平均较正常对照组、假手术组升高(P < 0.01)。 结论脓毒血症可造成病理学层面的小鼠肺组织损伤,致炎症因子表达升高,降低小鼠的生存率。通过观察该模型中反映肺损伤程度的相关指标的变化,可评估脓毒血症严重程度和研究损伤相关机制。 Abstract:ObjectiveTo explore the related mechanism of the lung injury of in the mouse model of sepsis constructed by cecal ligation and puncture. MethodsA total of 42 healthy male C57BL/6 mice were randomly divided into the control group, sham operation group and sepsis group(14 mice each group).The control group was not treated, the sham group was treated with cecal ligation, and the sepsis group was treated with cecal ligation combined with puncture.The lung tissue in three groups was collected after 24 hours of treatment, and the MSS score, survival rate, morphological change of lung tissue, score of lung injury, number of neutrophils and expression levels of tumor necrosis factor α(TNF-α) and interleukin-6(IL-6) in lung tissues were analyzed in three groups. ResultsThe MSS score, score of lung injury, number of neutrophils and expression levels of TNF-α and IL-6 in sepsis group were higher than those in control group and sham operation group(P < 0.01). ConclusionsSepsis can lead to the acute lung injury and increasing expression level of inflammatory factors, and decrease the survival rate of mice.The related indicator of reflecting lung tissue injury change can reflect the severity of sepsis, and study its related mechanism. -
表 1 3组相关指标比较(x±s)
分组 n MSS 肺组织损伤评分 炎性细胞 TNF-α IL-6 正常对照组 14 — 0.67±0.21 1 080±188.0 1.000±0.000 1.000±0.000 假手术组 14 4.14±0.27** 3.50±0.22** 2 699±285.6** 2.070±0.383* 1.578±0.084** 脓毒血症组 14 20.50±0.68**△△ 11.00±0.45**△△ 16 948±401.9**△△ 9.300±1.107**△△ 451.000±36.760**△△ F — 659.90 290.49 686.50 44.53 149.70 P — <0.01 <0.01 <0.01 <0.01 <0.01 MS组内 — 1 645.000 0.098 1.906×108 120.300 404 414.000 q检验:与正常对照组比较*P<0.05;**P<0.01,与假手术组比较△△P<0.01 -
[1] CHARCHAFLIEH J, WEI J, LABAZE G, et al.The role of complement system in septic shock[J].Clin Dev Immnol, 2012, 2012(2):407. [2] GAIESKI DF, EDWARDS JM, KALLAN MJ, et al.Benchmarking the incidence and mortality of severe sepsis in the United States[J].Crit Care Med, 2013, 41(5):1167. doi: 10.1097/CCM.0b013e31827c09f8 [3] SINGER M, DEUTSCHMAN CS, SEYMOUR CW, et al.The third international concensus definitions for sepsis and septic shock (sepsis-3)[J].JAMA, 2006, 315(8):801. [4] 张婷, 王祥瑞.脓毒血症休克的液体治疗[J].上海医药, 2011, 34(10):796. [5] SHRUM B, ANANTHA RV, XU SX, et al.A robust scoring system to evaluate sepsis severity in an animal model[J].BMC Res Notes, 2014, 7(12):233. [6] SHEHABI Y, BELLOMO R, READE MC, et al.Early intensive care sedation predicts long-term mortality in wentilated critically ill patients[J].Am J Respir Crit Care Med, 2012, 186(8):724. doi: 10.1164/rccm.201203-0522OC [7] KRESS JP, POHLMAN AS, O'CONNOR MF, et al.Daily interruption of sedative infusions in critically ill patients undergoing mechanical ventilation[J].N Engl J Med, 2000, 342(20):1471. doi: 10.1056/NEJM200005183422002 [8] FINK MP, WARREN HS, Strategies to improve drug developmengts for sepsis[J].Nat Rev Drug Discov, 2014, 13(10):741. doi: 10.1038/nrd4368 [9] MARSHALL JC, Why have clinical trials in sepsis failed?[J].Trends Mol Med, 2014, 20(4):195. doi: 10.1016/j.molmed.2014.01.007 [10] RITTIRSCH D, HUBER LANG MS, FLIERL MA, et al.Immunodesign of experimental sepsis by cecal ligation and puncture[J].Nat Protoc, 2009, 4(1):31. doi: 10.1038/nprot.2008.214 [11] NOVOTNY AR, REIM D, ASSFALG V, et al.Mixed antagonist response and sepsis severity-dependent dysbalance of pro- and anti-inflammatory responses at the onset postoperative sepsis[J].Immunobiology, 2012, 217(6):616. doi: 10.1016/j.imbio.2011.10.019 [12] PRAKASH PS, CALDWELL CC, LENTSCH AB, et al.Human microparticles generated during sepsis in patients with critical illness are neutrophil-derived and modulate the immune response[J].J Trauma Acute Care Surg, 2012, 73(2):401. doi: 10.1097/TA.0b013e31825a776d [13] MADDUX AB, DOUGLAS IS.Is the developmentally immature immune response in paediatric sepsis a recapitulation of immune tolerance?[J].Immunology, 2015, 145(1):1. [14] CHEN XH, YIN YJ, ZHANG JX.Sepsis and immune response[J].World J Emerg Med, 2011, 2(2):88. doi: 10.5847/wjem.j.1920-8642.2011.02.002 [15] NAMATH AI, PATTERSON AJ.Genetic polymorphisms in sepsis[J].Crit Care Clin, 2009, 25(4):835. doi: 10.1016/j.ccc.2009.06.004 [16] MEDINA E.Murine model of polymicrobial septic peritonitis using cecal ligation and puncture (CLP)[J].Methods Mol Biol, 2010, 602(2):411. [17] SEVRANSKY JE, LEVY MM, MARINI JJ.Mechanical ventilation in sepsis-induced acute lung injury/acute respiratory distress syndrome:an evidence-based review[J].Crit Care Med, 2004, 32(11 Suppl):S548. [18] ZEMANS RL, COLGAN SP, DOWNEY GP.Transepithelial migration of neutrophils:mechanisms and implications for acute lung injuiy[J].Am J Respir Cell Mol Biol, 2009, 40(5):519. doi: 10.1165/rcmb.2008-0348TR [19] KABAY B, KOCAEFE C, BAYKAL A, et al.Interleukin-10 gene transfer:prevention of multiple organ injury in a murine cecalligation and puncture model of sepsis[J].World J Surg, 2007, 31(1):105. doi: 10.1007/s00268-006-0066-9 [20] SADOWITZ B, ROY S, GATTO LA, et al.Lung injury induced by sepsis:lessons learned from large animal models and future directions for treatment[J].Expert Rev Anti Infect Ther, 2011, 9(12):1169. doi: 10.1586/eri.11.141 -




 下载:
下载: