-
卵巢癌是女性生殖器官最常见的三大恶性肿瘤之一,在妇科恶性肿瘤中发病率居第2位,其病死率居首位[1],其中卵巢浆液性癌占卵巢癌的75%。由于卵巢位置较深,早期病变不易发现,缺乏特异的早期临床表现及诊断方法,约70%的卵巢癌病人在发现时已属晚期,并有广泛的盆腔、腹腔、淋巴结转移或腹水形成[2]。
研究[3]表明,内质网应激(ERS)反应可能与肿瘤的发生、发展、转移及预后密切相关。而葡萄糖调节蛋白78(GRP78)是一种内质网分子伴侣,在ERS出现时其表达上调[4]。GRP78的主要功能包括促进新合成蛋白的折叠、聚集,识别内质网中的异常折叠蛋白并诱导其降解,充当内质网应激感受器等。随着对GRP78细胞内定位认识的不断深入,研究[5-6]发现除内质网外,肿瘤细胞表面也存在GRP78的表达。细胞表面GRP78被认为是一种受体样多功能蛋白,可以通过与不同的配体结合,在肿瘤细胞的增殖、凋亡、侵袭转移和耐药性中发挥重要的调节作用[7-8]。目前,细胞表面GRP78在调节肿瘤侵袭转移中的作用及可能的分子机制已成为研究的热点。本研究拟通过免疫组织化学法和Western blot检测GRP78在卵巢浆液性癌及卵巢浆液性囊腺瘤的表达情况,探讨GRP78在卵巢癌的发生发展、侵袭转移中的临床意义。
-
低转移潜能卵巢癌细胞HO-8910、高转移潜能卵巢癌细胞HO-8910PM购于上海通派生物科技公司。二甲基亚砜从Sigma-Aldrich公司购买。GRP78一抗以及二抗从Cell Signaling公司购买。shRNA-GRP78、pcDNA-GRP78和LipofectamineTM 2000均从上海吉玛基因公司购买。
收集2013年12月至2018年12月蚌埠医学院第二附属医院存档的60例卵巢浆液性癌组织及同时期40例卵巢浆液性囊腺瘤组织标本。卵巢癌病人年龄46~72岁;组织学类型均为浆液性腺癌;病理分级低级23例,高级37例;临床分期Ⅰ、Ⅱ期25例,Ⅲ、Ⅳ期35例;术后经病理证实有淋巴转移者13例,无淋巴转移者47例;有盆腔转移者36例,无盆腔转移者24例;盆腔外转移者19例,无盆腔外转移者41例。卵巢囊腺瘤病人年龄20~66岁,均为浆液性囊腺瘤。病例均经手术和病理确诊,术前均未接受放疗、化疗和免疫治疗等相关治疗,有完整临床及病理资料。
-
采用免疫组织化学法测定GRP78的表达,样本经10%甲醛固定,常规石蜡包埋,制成5 μm连续切片;然后依次经过脱蜡、脱苯、水化、抗原修复、封闭内源性过氧化物酶后,于室温下静置20 min,随后在4 ℃孵育一抗过夜。然后切片孵育带荧光标记的二抗,室温下孵育20 min,PBS洗片3次,每次5 min,滴加DAB显色溶液染色2 min,并将切片置于显微镜下观察显色结果;终止反应后以苏木素复染1 min,盐酸乙醇分化、脱水、二甲苯透明、中性树胶封片,待中性树胶干后,置于显微镜下观察拍片,并对阳性染色进行观察。对染色的细胞进行如下评分:显色细胞≤10%,为阴性(-);显色细胞>10%~25%,为阳性(+);显色细胞>25%~50%,为阳性(2+);显色的细胞≥50%,为阳性(3+)。按GRP78表达情况进行分层,显色阳性细胞<50%为低表达GRP78组,而显色阳性细胞≥50%为高表达GRP78组,比较2组卵巢浆液性癌病人临床指标之间的关系。
-
组织蛋白提取操作步骤如下:取-80 ℃保存的卵巢浆液性癌组织和卵巢浆液性囊腺瘤组织标本,在液氮下碾成粉状,冰上裂解30 min,匀质,1 000 r/min离心10 min,收集上清液。细胞蛋白提取操作如下:取生长状态良好的细胞,使用胰酶消化细胞,收集细胞悬液于4 mL的离心管中,2 500 r/min离心10 min,弃上层液体,加细胞裂解液,冰上裂解30 min,4 ℃、12 000 r/min离心收集样品。BCA法检测样品蛋白含量,蛋白定量后与上样缓冲液1:1混合,100 ℃煮沸5 min,变性的蛋白于-20 ℃保存。每道上样30 μg蛋白,经聚丙稀酰胺凝胶电泳后湿式转膜。PVDF膜放入5%脱脂奶粉中,室温封闭2 h,一抗4 ℃孵育过夜,二抗室温孵育2 h,最后在暗室中显影、定影、洗净、晾干。采用图像分析软件Gene Tools V3.04b分析蛋白条带灰度,以β-actin作为内参对照。
-
转染细胞分为3组:对照组、阴性对照组和shRNA-GRP78或pcDNA-GRP78组。依据试剂盒操作步骤,将细胞接种于6孔板中培养24 h,使用LipofectamineTM2000将shRNA-GRP78、pcDNA-GRP78分别转染至HO-8910细胞、HO-8910PM细胞,再加入无血清培养液培养6 h,吸去上述液体,加入正常培养基进行培养。
-
取对数生长期细胞接种于铺有30 μL Matrigel基质胶的Transwell板上室。下室为600 μL含10%胎牛血清的RPMI 1640培养基。常规培养48 h后,用棉签擦去上层细胞,下层细胞用4%多聚甲醛固定并用结晶紫染色。将固定染色的细胞置于倒置显微镜下观察拍照,任选5个视野进行计数,取平均值。
-
采用两独立样本t检验、χ2检验、方差分析和q检验。
-
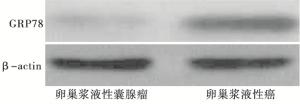
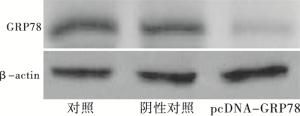
免疫组织化学结果显示,GRP78蛋白定位于细胞质中,呈棕黄色颗粒(见图 1),40例卵巢浆液性囊腺瘤组织中GRP78阴性表达30例(75%),GRP78阳性表达10例(25%),60例卵巢浆液性癌组织中GRP78阴性表达6例(10%),阳性表达54例(90%);卵巢浆液性癌组织中GRP78阳性表达明显高于卵巢浆液性囊腺瘤组织(χ2=44.01,P<0.01)。Western blotting结果显示,GRP78在卵巢浆液性癌组织的蛋白表达明显高于卵巢浆液性囊腺瘤组织(见图 2)。
-
GRP78的表达量与病人的病理分级相关,GRP78表达量越高,卵巢浆液性癌病人病理分级程度越高,临床病理分期分析结果与病理分级结果一致。且与低表达GRP78的卵巢癌病人相比,高表达GRP78组的病人,糖类抗原125(CA125)指标更高。发生淋巴结转移、盆腔转移、盆腔外转移的比例更高(P<0.01)(见表 1)。
项目 GRP78表达量<50%(n=28) GRP78表达量≥50%(n=32) χ2 P 年龄/岁 57.57±11.15 60.16±11.34 -0.89* >0.05 肿瘤直径/cm 11.00±6.12 13.54±5.24 -1.10* >0.05 CA125/(U/mL) 144.00±121.25 647.31±499.98 -5.51* <0.01 病理分级 低级
高级20(86.92)
8(21.63)3(13.17)
29(78.43)24.33 <0.01 临床病理分期 Ⅰ、Ⅱ期
Ⅲ、Ⅳ期22(88.01)
6(17.12)3(12.04)
29(82.93)29.42 <0.01 淋巴结转移 无
有28(60.93)
0(0.02)18(39.17)
14(100.01)15.98 <0.01 盆腔转移 无
有22(91.76)
6(16.75)2(8.34)30
(83.33)32.54 <0.01 盆腔外转移 无
无25(62.06)
3(15.83)16(38.02)
16(84.28)10.65 0.01 *示t值 表 1 浆液性卵巢癌临床指标与GRP78的表达水平的关系[n;百分率(%)]
-
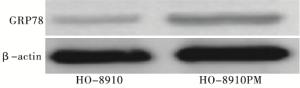
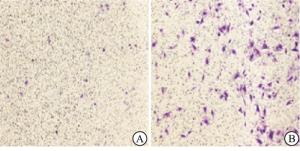
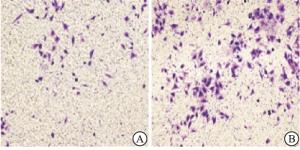
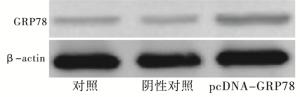
结果显示,与HO-8910细胞比较,HO-8910PM细胞中GRP78的表达明显增加(见图 3)。Transwell法检测结果表明,与HO-8910细胞比较,HO-8910PM细胞的侵袭、迁移能力明显升高(见图 4~5、表 2)(P<0.01)。
分组 侵袭细胞数 迁移细胞数 HO-8910细胞 34.20±8.23 16.60±6.35 HO-8910PM细胞 113.00±14.21 69.40±4.16 t -10.73 -15.56 P <0.01 <0.01 表 2 HO-8910和HO-8910PM细胞侵袭、迁移能力比较(n=3;x±s)
-
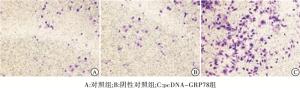
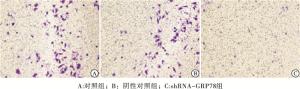
在HO-8910细胞中过表达GRP78,细胞的侵袭、迁移能力明显升高(P<0.01)(见图 6~8、表 3)。而在HO-8910PM细胞中干扰GRP78的表达,细胞的侵袭、迁移能力明显降低(P<0.01)(见图 9~11、表 4)。
分组 侵袭细胞数 迁移细胞数 对照组 34.20±8.23 16.60±6.35 阴性对照组 34.40±9.56 17.80±5.98 pcDNA-GRP78组 108.60±18.89 64.80±10.35 F 53.51 61.86 P <0.01 <0.01 MS组内 9 200.867 3 778.067 表 3 过表达GRP78对HO-8910细胞侵袭、迁移能力的影响(n=3;x±s)
分组 侵袭细胞数 迁移细胞数 对照组 111.40±14.28 69.40±4.16 阴性对照组 106.00±6.33 66.40±8.30 shRNA-GRP78组 39.80±8.44 19.80±5.68 F 75.70 98.07 P <0.01 <0.01 MS组内 7 948.467 3 867.267 表 4 下调GRP78表达对HO-8910PM细胞侵袭、迁移能力的影响(n=3;x±s)
-
正常细胞在缺氧、酸中毒等应激状态下会产生ERS,ERS可导致细胞内GRP78含量增加,使细胞的耐受性增强,保护细胞抵抗有害刺激的损伤,保持内环境稳态[9]。在肿瘤细胞中,ERS成为其主要反应方式,从而导致GRP78持续升高,使肿瘤细胞对缺氧、酸中毒等因素的耐受性增加[10]。GRP78高表达存在于多种肿瘤中,包括泌尿系、消化系、乳腺、脑和呼吸系统肿瘤等[11]。ZHANG等[12]在消化系统肿瘤研究中发现,GRP78的表达升高与胃癌的淋巴结转移呈正相关关系,并导致病人的不良预后。使用RNAi技术定向下调GRP78表达,可明显降低胃癌细胞的淋巴转移能力。同样在头颈部肿瘤研究中,CHIU等[13]以RNAi技术定向基因敲除GRP78在多个头颈部鳞癌培养细胞系中的表达发现,在基因敲除鳞癌细胞系中,反映肿瘤转移能力的局部细胞克隆团块形成能力从53%下降至12%,并且在原位体外肿瘤转移抑制率可达到67%,抑制肝转移率降低约90%。
本研究检测了GRP78在卵巢浆液性癌及卵巢浆液性囊腺瘤标本中的表达,免疫组织化学检测结果显示卵巢浆液性癌组织中GRP78阳性细胞的比例明显高于卵巢浆液性囊腺瘤组织。在本研究中,首次观察到了GRP78表达量高的卵巢浆液性癌病人,肿瘤分级和临床病理分期更高,CA125水平更高、肿瘤体积更大。且GRP78表达量高的病人,发生淋巴结转移、盆腔转移、盆腔外转移所占比例更高。以上结果说明GRP78可能为卵巢癌病人重要的预后因子。
体外研究中,Western blot结果显示,与转移潜能低的HO-8910细胞相比,转移潜能高的HO-8910PM细胞GRP78表达明显升高。在HO-8910细胞中过表达GRP78,细胞发生侵袭、迁移能力增强;相反,在HO-8910PM细胞中沉默GRP78可以降低细胞的侵袭、迁移能力。
本研究仅揭示了GRP78可促进卵巢癌的侵袭、迁移,但GRP78如何促进卵巢癌的转移尚不清楚。有研究报道,GRP78的表达水平与肝癌细胞的恶性程度呈正相关关系,它通过激活FAK及MMP-2促进肝癌的侵袭转移[14-15]。在前列腺癌中,GRP78与活化的α2巨球蛋白结合,激活PAK2,导致LIMK和Cofillin磷酸化,从而促进肿瘤细胞的增殖、侵袭和转移;在人畸胎瘤和乳腺癌中,GRP78与Cripto-1直接结合,抑制TGF-β介导的Smad2/3磷酸化,激活MAPK/PI3K信号通路,下调E-cadherin的表达,促进肿瘤细胞增殖、侵袭和转移;在结肠癌中,GRP78与β1- Integrin结合,活化FAK,激活尿激酶型纤溶酶原,促进细胞外基质的降解,调节肿瘤侵袭和转移[16-18]。
总之,该研究揭示了GRP78可以影响卵巢癌细胞的侵袭迁移能力,提示GRP78可能是卵巢癌病人重要的预后因子之一,但还需要体内实验和对病人随访进一步证实。
葡萄糖调节蛋白78在卵巢癌侵袭转移中的作用
Role of glucose-regulated protein 78 in the invasion and metastasis of ovarian cancer
-
摘要:
目的探讨葡萄糖调节蛋白78(GRP78)在卵巢癌侵袭转移中的作用。 方法免疫组织化学法检测60例卵巢浆液性癌和40例卵巢浆液性囊腺瘤组织中GRP78的表达情况,Western blotting法检测GRP78的表达水平,分析GRP78的表达与卵巢浆液性癌临床病理指标之间的关系。采用Transwell小室法检测HO-8910细胞和HO-8910PM细胞侵袭、迁移能力;分别使用shRNA-GRP78干扰和pcDNA-GRP78过表达GRP78检测HO-8910PM细胞和HO-8910细胞侵袭、迁移能力的变化。 结果免疫组织化学结果显示,GRP78在卵巢浆液性癌组织中的阳性表达率为90%,明显高于卵巢浆液性囊腺瘤的25%(P<0.01)。GRP78在卵巢浆液性癌组织中表达水平高于卵巢浆液性囊腺瘤组织。GRP78表达水平高的卵巢浆液性癌病人,临床病理分级、分期更高,糖类抗原125水平更高,且发生淋巴结转移、盆腔转移、盆腔外转移的病人比例更高(P<0.01)。体外研究结果显示,GRP78在高转移潜能的HO-8910PM细胞中的表达明显高于低转移潜能的HO-8910细胞(P<0.01)。在HO-8910细胞中过表达GRP78可明显促进细胞的侵袭、迁移能力,而在HO-8910PM细胞中干扰GRP78的表达可明显降低细胞的侵袭、迁移潜能(P<0.01)。 结论卵巢癌组织中GRP78可促进卵巢癌细胞的侵袭、迁移能力。 Abstract:ObjectiveTo investigate the role of glucose-regulated protein 78(GRP78) in the invasion and metastasis of ovarian cancer. MethodsThe expression levels of GRP78 in 60 ovarian serous carcinoma and 40 ovarian serous cystadenoma tissues were detected using the immunohistochemistry(IHC) and Western blotting.The relationship between the clinical indicators of ovarian serous carcinoma and GRP78 expression was analyzed.The invasion and migration ability of HO-8910 cells and HO-8910PM cells were detected using Transwell assay.The invasion and migration ability of HO-8910 cells and HO-8910PM cells treated with shRNA-GRP78 interference and pcDNA-GRP78 overexpression were detected, respectively. ResultsThe results of IHC showed that the positive expression rate of GRP78 in ovarian serous carcinoma tissues(90%) was significantly higher than that in ovarian serous cystadenoma tissues(25%)(P < 0.01).The results of Western blot showed that the expression level of GRP78 in ovarian serous carcinoma tissue was significantly higher than that in ovarian serous cystadenoma tissue.Among the ovarian serous carcinoma patients with high GRP78 expression level, the clinicopathological grade and stage and carbohydrate antigen 125 level were higher, and the proportion of patients with lymph node metastasis, pelvic metastasis, and external pelvic metastasis was higher(P < 0.01).The results of in vitro studies showed that the expression level of GRP78 in HO-8910PM cells with high metastatic potential was significantly higher than that in HO-8910 cells with low metastatic potential(P < 0.01).The overexpression of GRP78 in HO-8910 cells could promote the invasion and migration ability of the cells, while silencing GRP78 expression in HO-8910PM cells could significantly reduce the invasion and migration potential of the cells(P < 0.01). ConclusionsGRP78 can promote the invasion and migration potential of ovarian cancer cells. -
Key words:
- ovarian neoplasms /
- glucose-regulated protein 78 /
- invasion /
- metastasis
-
表 1 浆液性卵巢癌临床指标与GRP78的表达水平的关系[n;百分率(%)]
项目 GRP78表达量<50%(n=28) GRP78表达量≥50%(n=32) χ2 P 年龄/岁 57.57±11.15 60.16±11.34 -0.89* >0.05 肿瘤直径/cm 11.00±6.12 13.54±5.24 -1.10* >0.05 CA125/(U/mL) 144.00±121.25 647.31±499.98 -5.51* <0.01 病理分级 低级
高级20(86.92)
8(21.63)3(13.17)
29(78.43)24.33 <0.01 临床病理分期 Ⅰ、Ⅱ期
Ⅲ、Ⅳ期22(88.01)
6(17.12)3(12.04)
29(82.93)29.42 <0.01 淋巴结转移 无
有28(60.93)
0(0.02)18(39.17)
14(100.01)15.98 <0.01 盆腔转移 无
有22(91.76)
6(16.75)2(8.34)30
(83.33)32.54 <0.01 盆腔外转移 无
无25(62.06)
3(15.83)16(38.02)
16(84.28)10.65 0.01 *示t值 表 2 HO-8910和HO-8910PM细胞侵袭、迁移能力比较(n=3;x±s)
分组 侵袭细胞数 迁移细胞数 HO-8910细胞 34.20±8.23 16.60±6.35 HO-8910PM细胞 113.00±14.21 69.40±4.16 t -10.73 -15.56 P <0.01 <0.01 表 3 过表达GRP78对HO-8910细胞侵袭、迁移能力的影响(n=3;x±s)
分组 侵袭细胞数 迁移细胞数 对照组 34.20±8.23 16.60±6.35 阴性对照组 34.40±9.56 17.80±5.98 pcDNA-GRP78组 108.60±18.89 64.80±10.35 F 53.51 61.86 P <0.01 <0.01 MS组内 9 200.867 3 778.067 表 4 下调GRP78表达对HO-8910PM细胞侵袭、迁移能力的影响(n=3;x±s)
分组 侵袭细胞数 迁移细胞数 对照组 111.40±14.28 69.40±4.16 阴性对照组 106.00±6.33 66.40±8.30 shRNA-GRP78组 39.80±8.44 19.80±5.68 F 75.70 98.07 P <0.01 <0.01 MS组内 7 948.467 3 867.267 -
[1] 张骞, 李力.循环肿瘤细胞在卵巢癌预测和预后中的应用价值[J].国际妇产科学杂志, 2018, 45(6):609. doi: 10.3969/j.issn.1674-1870.2018.06.002 [2] 孙晶.健脾生血汤联合静脉、腹腔双途径化疗治疗45例晚期卵巢癌并发腹水患者的疗效分析[J].首都食品与医药, 2018, 25(19):31. doi: 10.3969/j.issn.1005-8257.2018.19.026 [3] 张旭明, 王胜超, 黄尤光.内质网应激与肿瘤关系的研究进展[J].生命的化学, 2018, 38(5):743. [4] 华正伟, 侯君妍, 汲坤.葡萄糖调节蛋白78与肿瘤相关性的研究进展[J].沈阳医学院学报, 2015, 17(1):50. doi: 10.3969/j.issn.1008-2344.2015.01.019 [5] ZHANG Y, LIU R, NI M, et al.Cell surface relocalization of the endoplasmic reticulum chaperone and unfolded protein response regulator GRP78/BiP[J].J Biol Chem, 2010, 285(20):15065. doi: 10.1074/jbc.M109.087445 [6] WANG M, WEY S, ZHANG Y, et al.Role of the unfolded protein response regulator GRP78/BiP in development, cancer, and neurological disorders[J].Antioxid Redox Signal, 2009, 11(9):2307. doi: 10.1089/ars.2009.2485 [7] HARDY B, RAITER A, YAKIMOV M, et al.Colon cancer cells expressing cell surface GRP78 as a marker for reduced tumorigenicity[J].Cell Oncol(Dordr), 2012, 35(5):345. doi: 10.1007/s13402-012-0094-4 [8] RAY R, DE RIDDER GG, EU JP, et al.The Escherichia coli subtilase cytotoxin A subunit specifically cleaves cell-surface GRP78 protein and abolishes COOH-terminal-dependent signaling[J].J Biol Chem, 2012, 287(39):32755. doi: 10.1074/jbc.M112.399808 [9] FRANCO-CHUAIRE ML, MAGDA CAROLINA SC, CHUAIRE-NOACK L.Epithelial-mesenchymal transition(EMT):principles and clinical impact in cancer therapy[J].Invest Clin, 2013, 54(2):186. [10] HART LS, El-DEIRY WS.Cell death:a new Par-4 the TRAIL[J].Cell, 2009, 138(2):220. doi: 10.1016/j.cell.2009.07.007 [11] 范丽梅.GRP78在卵巢癌中的表达及其对卵巢癌细胞顺铂耐药的影响[D].长春: 吉林大学, 2011. [12] ZHANG J, JIANG Y, JIA Z, et al.Association of elevated GRP78 expression with increased lymph node metastasis and poor prognosis in patients with gastric cancer[J].Clin Exp Metastasis, 2006, 23(7/8):401. [13] CHIU CC, LIN CY, LEE LY, et al.Glucose-regulated protein 78 regulates multiple malignant phenotypes in head and neck cancer and may serve as a molecular target of therapeutic intervention[J].Mol Cancer Ther, 2008, 7(9):2788. doi: 10.1158/1535-7163.MCT-08-0172 [14] SU R, LI Z, LI H, et al.Grp78 promotes the invasion of hepatocellular carcinoma[J].BMC Cancer, 2010, 10(1):20. doi: 10.1186/1471-2407-10-20 [15] LI H, SONG H, LUO J, et al.Knockdown of glucose-regulated protein 78 decreases the invasion, metalloproteinase expression and ECM degradation in hepatocellular carcinoma cells[J].J Exp Clin Cancer Res, 2012, 31(1):39. doi: 10.1186/1756-9966-31-39 [16] MIHARADA K, KARLSSON G, REHN M, et al.Cripto regulates hematopoietic stem cells as a hypoxic-niche-related factor through cell surface receptor GRP78[J].Cell Stem Cell, 2011, 9(4):330. doi: 10.1016/j.stem.2011.07.016 [17] WANG W, GOSWAMI S, SAHAI E, et al.Tumor cells caught in the act of invading:their strategy for enhanced cell motility[J].Trends Cell Biol, 2005, 15(3):138. doi: 10.1016/j.tcb.2005.01.003 [18] KELBER JA, PANOPOULOS AD, SHANI G, et al.Blockade of Cripto binding to cell surface GRP78 inhibits oncogenic Cripto signaling via MAPK/PI3K and Smad2/3 pathways[J].Oncogene, 2009, 28(24):2324. doi: 10.1038/onc.2009.97 -





 下载:
下载: