-
鼻咽癌是最常见的头颈部肿瘤之一。2018年在世界范围内有13万人确诊为鼻咽癌,在中国发病率更是高达9.8/10万,其中70%的病人为局部晚期鼻咽癌[1-2]。由于鼻咽部特殊的解剖结构以及鼻咽癌对放射线敏感等生物学特性,决定了放射治疗是鼻咽癌首选的治疗方式[3]。而对于局部晚期鼻咽癌,同步放化疗是其标准的治疗方式[4]。近年来,随着放疗设备及放疗技术的快速发展,鼻咽癌放疗的5年总生存已超过80%[5]。然而,口干等放疗不良反应仍然是影响病人放疗后生活质量的主要因素。如何降低鼻咽癌放疗不良反应是近年来研究的热点之一。螺旋断层放疗(helical tomotherapy,HT)是近年来应用于临床最先进的调强放疗技术之一。HT作为一种新兴的调强放射治疗技术,集普通调强放疗(intensity-modulated radiation therapy,IMRT)、影像引导调强适形放疗、剂量引导调强适形放疗于一体,把螺旋断层CT与直线加速器进行了完美结合,能在CT引导下360°聚焦断层照射肿瘤,实现真正的动态调强。关于HT在鼻咽癌放疗中的研究,国内外报道相对较少,且存在样本量偏少甚至研究结果不尽一致的地方[6-8]。本研究旨在比较HT和IMRT在靶区适形度指数、均匀性指数、急性不良反应以及近期疗效上的差异,评估HT在局部晚期鼻咽癌放疗上的优势。现作报道。
-
收集2017年2月至2019年9月我科收治的局部晚期鼻咽癌病人140例(Ⅲ~Ⅳa期,AJCC第八版分期),年龄12~83岁。纳入标准: (1)病理诊断明确; (2)临床资料完整; (3)临床分期为Ⅲa~Ⅳb期; (4)卡氏评分≥70分; (5)无放化疗禁忌;(6)签署放化疗同意书。根据病人放疗设备的不同分为HT组和IMRT组,各70例。2组病人一般资料比较差异均无统计学意义(P>0.05) (见表 1)。
分组 n 男 女 年龄/岁 病理类型 分期/期 鳞状细胞癌 分化性非角化性癌 未分化癌 Ⅲ Ⅳa HT组 70 54 16 49.63±14.70 10 25 35 37 33 IMRT组 70 55 15 53.19±12.58 8 23 39 41 29 χ2 — 0.04 1.54* 0.52 0.46 P — >0.05 >0.05 >0.05 >0.05 *示t值 表 1 2组基线资料比较(n)
-
病人仰卧体位,采用热塑头颈肩一体面罩固定头颈部,后在CT模拟机下进行模拟定位。扫描范围为自头顶皮肤向下扫描至锁骨头下缘下5 cm,层厚为3 mm。
-
靶区勾画参照ICRU 50号及62号报告的标准,依据病人头颈部磁共振成像(MRI)将鼻咽部肿瘤定义为GTVnx,转移淋巴结定义为GTVnd。GTVnx及GTVnd分别外扩3 mm命名为PGTVnxp和PGTVnd;CTV1为高危区域,包括pGTVnx,以及整个鼻咽部、咽旁间隙、咽后淋巴结区域、颅底、斜坡、蝶窦、翼腭窝、鼻腔及上颌窦后壁前5 mm、部分口咽及上颈部淋巴引流区。CTV2为低危区域,也是预防照射区,主要包括下颈部淋巴引流区。CTVl及CTV2分别外扩3 mm生成PTV1和PTV2,与皮肤保持至少3 mm距离以保护皮肤。危及器官主要包括垂体、脑干、眼球、晶体、视神经、视交叉、颞颌关节、内耳、腮腺、口腔、脊髓等。如果原发肿瘤或者转移淋巴结体积较大,放疗期间根据肿瘤退缩情况会进行再次CT模拟定位及靶区勾画。
-
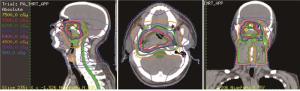
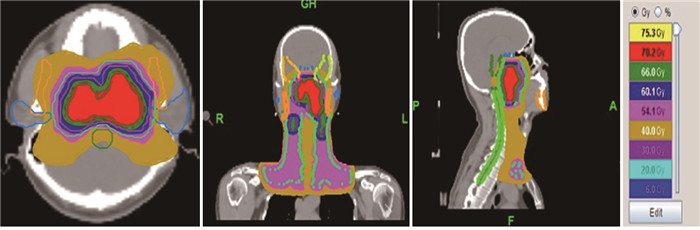
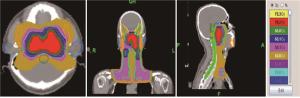
PGTVnx的处方剂量为69.96 Gy/33F,PGTVnd处方剂量为66~70 Gy/33F,PTV1为60 Gy/33F,PTV2为54 Gy/33F,同时要求处方剂量至少覆盖98%的靶体积,并且>110%处方剂量的体积<20%,>93%的处方剂量的体积<3%。根据RTOG标准限制危及器官剂量:腮腺V30<50%、颞叶<60 Gy、脑干<54 Gy、脊髓<45 Gy、视神经及视交叉<54 Gy、颞颌关节<60 Gy、晶体剂量<5 Gy、内耳<50 Gy。医师先应用Pinnacle 9.8系统进行靶区及危及器官的勾画,后填写放疗计划申请单。申请单包括处方剂量及危及器官限制剂量。物理师通过HiArt TomoTherapy工作站进行HT放疗计划的设计及验证,而IMRT计划则通过Pinnacle 9.8系统完成。HT组和IMRT组放疗计划的部分等剂量线分布图见图 1~2。
-
2个治疗组在放疗期间均给予顺铂为基础的同步化疗,顺铂剂量为80 mg/m2,3周为一个周期。化疗期间辅助给予止吐药及保护胃肠道黏膜药物。
-
CN=TVRI/TV×TVRI/VRI, 公式中的TVRI为参考等剂量曲线所包绕的靶体积,VRI为参考等剂量曲线包绕的所有区域的体积。CN值越接趋近于1说明肿瘤靶区的适形度越好。
-
HI=D5/D95,公式中D5为包绕5%计划靶区的最低剂量,D95为包绕95%计划靶区的最低剂量,数值越趋近于1则靶区的均匀性越好。
-
所有病人治疗期间每周行血常规检查,2~3周行肝肾功能检查,放疗结束后1个月复查头颈部增强磁共振及上腹部彩超等评价病人近期疗效。
-
采用最常用的美国肿瘤放射治疗组(Radiation Therapy Oncology Group,RTOG)/欧洲癌症治疗研究组织(European Organization for Research on Treatment of Cancer,EORTC)标准[9]进行评价。
-
根据实体瘤评价标准RECTST1.1[10],比较2组病人完全缓解(CR)、部分缓解(PR)、病情稳定(SD)、病情进展(PD)、客观有效率(ORR)及不良反应发生率等相关疗效评价指标。ORR=(CR例数+PR例数)/总例数×100%;近期疗效的观察时间从放疗开始第1天至放疗结束后1个月。
-
采用t(或t′)检验、χ2检验和秩和检验。
-
除PGTVnx中HI差异无统计学意义外(P>0.05),HT组在靶区CN和HI上均优于IMRT组(P<0.05~P<0.01)(见表 2)。
分组 n PGTVnx PGTVnd PTV1 PTV2 CN HI CN HI CN HI CN HI HT组 70 0.91±0.01 1.06±0.01 0.91±0.02 1.08±0.04 0.90±0.02 1.19±0.02 0.89±0.03 1.08±0.02 IMRT组 70 0.90±0.03 1.06±0.01 0.88±0.04 1.02±0.03 0.86±0.03 1.21±0.03 0.84±0.02 1.09±0.02 t — 2.65* 0.00 5.61* 10.04* 9.28* 4.64* 11.60* 2.96 P — <0.05 >0.05 <0.01 <0.01 <0.01 <0.01 <0.01 <0.01 *示t′值 表 2 HT组与IMRT组靶区CN和HI比较
-
2组病人危及器官中除了视神经、视交叉以下颌骨外,其他危及器官的最大剂量和平均剂量比较中HT组均优于IMRT组(P<0.05~P<0.01)(见表 3)。
分组 n 眼球 晶体 视神经 视交叉 脑干 脊髓 腮腺 内耳 口腔 下颌骨 最大剂量 HT组 70 20.26±6.21 3.92±1.78 31.58±14.65 33.32±12.78 51.08±5.26 37.08±3.22 71.46±2.98 54.19±3.37 61.90±11.13 61.45±7.65 MRT组 70 22.92±7.22 4.68±0.45 32.88±7.91 34.87±16.76 54.10±2.55 41.88±2.04 74.02±2.89 56.09±2.21 67.29±9.78 63.65±5.90 t — 2.34 3.46* 0.65* 0.62* 4.32* 10.54* 5.16 3.94* 3.04 1.91 P — <0.05 <0.01 >0.05 >0.05 <0.01 <0.01 <0.01 <0.01 <0.01 >0.05 平均剂量 HT组 70 5.02±1.42 2.85±1.33 24.54±8.81 27.76±9.91 34.56±5.36 27.02±5.04 35.77±3.55 38.90±3.47 31.18±7.06 46.19±8.77 MRT组 70 6.05±2.10 4.54±0.75 26.65±7.10 28.32±12.42 37.12±6.10 30.07±2.11 39.09±2.02 47.63±3.65 39.62±6.35 43.71±6.67 t — 3.40* 9.26* 1.56 0.29 2.64 4.67* 6.80* 14.50 7.44 1.88* P — <0.05 <0.01 >0.05 >0.05 <0.01 <0.01 <0.01 <0.01 <0.01 >0.05 *示t′值 表 3 HT组与IMRT组计划中危及器官的最大和平均剂量比较(x±s; Gy)
-
据RTOG/EORTC急性放射反应标准,2组病人发生于口腔黏膜、唾液腺等大部分器官损伤的急性不良反应主要为Ⅰ~Ⅱ级,极少数病人出现3级反应。发生较重的Ⅲ、Ⅳ级不良反应的主要表现为白细胞减少和皮肤损伤。HT组病人在急性腮腺损伤和听力损伤保护方面优于IMRT组(P<0.05~P<0.01)(见表 4)。2组其他急性不良反应差异均无统计学意义(P>0.05)。
分组 n 0级 Ⅰ级 Ⅱ级 Ⅲ级 Ⅳ级 uc P 口腔黏膜炎 140 0 29 74 36 1 0.15 >0.05 HT组 70 0 11 43 16 0 IMRT组 70 0 18 31 20 1 耳鸣 120 104 10 5 1 0 2.17 <0.05 HT组 60 56 3 1 0 0 IMRT组 60 48 7 4 1 0 腮腺损伤 140 9 73 58 0 0 4.87 <0.01 HT组 70 9 45 16 0 0 IMRT组 70 0 28 42 0 0 放射性皮炎 140 1 19 96 23 1 0.60 >0.05 HT组 70 1 8 48 12 1 IMRT组 70 0 11 48 11 0 咽喉疼痛 140 9 115 13 3 0 1.42 >0.05 HT组 70 5 60 4 1 0 IMRT组 70 4 55 9 2 0 消化系统反应 140 9 97 29 5 0 0.47 >0.05 HT组 70 4 51 12 3 0 IMRT组 70 5 46 17 2 0 白细胞减少 140 46 16 47 21 10 1.45 >0.05 HT组 70 26 9 22 10 3 IMRT组 70 20 7 25 11 7 血小板降低 140 101 27 9 3 0 0.49 >0.05 HT组 70 52 12 4 2 0 IMRT组 70 49 15 5 1 0 肝功能损伤 140 127 8 5 0 0 0.82 >0.05 HT组 70 62 6 2 0 0 IMRT组 70 65 2 3 0 0 肾功能损伤 140 135 4 1 0 0 0.49 >0.05 HT组 70 68 2 0 0 0 IMRT组 70 67 2 1 0 0 疲劳 140 7 92 41 0 0 1.04 >0.05 HT组 70 4 42 24 0 0 IMRT组 70 3 50 17 0 0 体质量减轻 122 35 55 24 8 0 0.68 >0.05 HT组 70 20 30 12 8 0 IMRT组 52 15 25 12 0 0 表 4 HT组与IMRT组病人不良反应比较(n)
-
2组近期疗效比较差异无统计学意义(P>0.05)(见表 5)。
分组 n CR PR SD PD ORR/% uc P HT组 70 44 22 4 0 94.29 0.71 >0.05 IMRT组 70 40 25 4 1 92.86 合计 140 84 47 8 1 93.57 表 5 HT组与IMRT组病人近期疗效比较(n)
-
鼻咽癌是我国最多见的头颈部肿瘤之一,在我国的华南地区尤其高发[1]。随着放疗技术的进步及放疗设备的发展,鼻咽癌的5年生存率达到了80%以上[5]。放疗靶区的适形度及均匀性是决定放疗疗效的关键因素。放射性腮腺损伤等放疗所致并发症是影响病人放疗后生活质量的主要因素。如何提高靶区的适形度等以及降低放疗带来的不良反应以提高病人放疗后的生活质量是目前鼻咽癌治疗方面最需关注的问题,也是近年来研究的热点。PUEBLA等[11]通过对17例局部晚期鼻咽癌病人行HT放疗研究显示,HT在剂量学上较普通IMRT有靶区适形度及剂量均匀性,同时又显著降低了周围重要器官的受照剂量。ZHANG等[12]针对局部晚期鼻咽癌病人进行了三维适形放射治疗计划与Tomotherapy计划剂量学的比较,结果显示采用螺旋断层放疗更能进一步改善放疗靶区的适形度和均匀度,对正常组织实现更好的保护。但该研究入组HT放疗的病人数较少。本研究中,我们对入组的70例病人HT放疗情况进行了分析,研究结果显示在处方剂量(PGTVnx)中,HT组在靶区HI上与IMRT组无统计学意义,其余变量中HT组在靶区CN和HI上均优于IMRT组(P<0.05)。同时我们也比较了HT组与IMRT组放疗计划中危及器官的最大剂量和平均剂量的差别,2组病人中除了视神经、视交叉以及下颌骨无明显异常外,腮腺、内耳等其他危及器官的最大剂量和平均剂量比较中HT组均优于IMRT组。提示在鼻咽癌放疗上HT相较于普通IMRT有较大的放射物相关的剂量学优势。
目前鼻咽癌的放射治疗总体已达到较高的肿瘤控制率。因此,如何更好地保护靶区内肿瘤周围的正常组织器官降低放疗反应以提高病人放疗后的生活质量具有重要的意义。相较于二维时代的普通放疗,三维适形放疗及调强放疗的出现使危及器官的保护得到很大的改善,降低了放疗反应。本研究结果表明,2组病人发生于口腔黏膜、唾液腺等大部分器官损伤的急性不良反应主要为Ⅰ~Ⅱ级,极少数病人出现Ⅲ级反应,均在可控范围内。发生较重的Ⅲ级及Ⅳ级不良反应的主要表现为少数病人白细胞减少和极少数病人的皮肤损伤。放射性腮腺损伤会影响腮腺的分泌功能,引起口干等症状,是鼻咽癌放疗后生活质量下降的主要原因,所以对于腮腺的保护尤为重要[13]。HT可能会使腮腺等危及器官的受照射剂量进一步下降。文献[14-15]报道了鼻咽癌等头颈部肿瘤螺旋断层放疗计划中危及器官保护方面的研究,发现Tomotherapy在满足临床要求的靶区剂量前提下比常规调强放疗更能降低腮腺等周围危及器官的受照射剂量。LEUNG等[16]分析72例局部晚期鼻咽癌螺旋断层放疗的治疗情况,仅有2例病人出现Ⅱ级口干,显示HT具有较好的腮腺保护作用。本研究结果显示HT组Ⅰ~Ⅱ级腮腺损伤病人61例,而IMRT组70例,2组比较差异有统计学意义(P<0.05)。提示HT放疗确实进一步降低了腮腺损伤的发生率和发生程度。尽管HT放疗显示出较好的剂量学优势及对腮腺良好的保护,但HT放疗局部晚期鼻咽癌病人中急性放射性腮腺损伤的发生率仍不低。实际上,腮腺在接受放射线照射后体积会发生较大变化,放疗后期腮腺甚至缩小30%以上[17-18]。缩小的腮腺会进一步向体中线位移从而导致腮腺实际接受的射线量大于生成放疗计划时的腮腺受量。所以,尽管HT对腮腺进行了很好的保护,但想完全避免急性放射性腮腺炎的发生目前尚不现实。由于鼻咽癌放疗过程中通常会使内耳结构包括在较高剂量的照射野内,故不同程度的听力损伤是鼻咽癌放疗引起的较为常见的不良反应。同时同步化疗会增加听力损伤的发生。BHANDARE等[19]研究显示鼻咽癌同步放化疗病人5年感音神经性耳聋的发生率由单纯放疗的8%上升至30%。所以如何进一步降低内耳的受照射剂量对于听力损伤的保护具有重要的意义。目前针对内耳的剂量限制还存在较大差异,Dmean<50 Gy是目前比较常用的限定剂量[20]。本研究结果显示,HT组病人内耳的平均剂量为(38.900±3.470) Gy,而IMRT组为(47.625±3.651) Gy,表明HT在听力保护上有较好的优势(P<0.05)。然而HT在口腔黏膜反应及咽喉疼痛等方面未表现出明显的优势,可能与口腔及咽喉部黏膜炎症的阈值较低有关。同步放化疗是局部晚期鼻咽癌标准的治疗方案,但同时同步化疗也加重了病人的放疗反应[12]。最严重的表现是白细胞减少,少数病人出现Ⅲ~Ⅳ级的白细胞降低。因而体质较弱或年龄较大的局部晚期鼻咽癌病人未能按既定方案完成同步化疗。在粒细胞集落刺激因子的应用下,所有病人均完成了放疗计划。本研究中,主要由同步化疗引起的胃肠道、肝肾功能及白细胞毒性等方面,2组未见明显异常(P>0.05)。HT组病人在减轻不良反应方面具有一定优势,使病人在放疗期间的依从性得到提高。同时2组病人放疗后疲乏及体质量下降程度差异均无统计学意义(P>0.05),分析认为乏力及体质量下降主要与病人的饮食有关,而2组病人口腔溃疡反应及化疗引起的胃肠道反应无明显异常。
在近期疗效的方面,2组病人的差异无统计学意义(P<0.05),该结果与文献[21]一致。这说明HT在剂量学以及危及器官保护上的优势尚未转化成近期疗效的提高。HT组病人放疗后KPS评分相比普通IMRT组有一定提高。这可能与HT组病人腮腺等危及器官损伤较轻,病人在放疗后机体状况得到较快恢复有关。
本研究也有几个不足之处。第一,因随访时间较短,尚未有无进展生存时间及总生存时间方面的数据。第二,本研究是样本量偏少。在下一步的工作中会继续扩充样本量,进一步观察病人的晚期不良反应及远期疗效,更客观地评价螺旋断层放疗在鼻咽癌放疗中的价值。
综上所述,相比普通IMRT,HT在局部晚期鼻咽癌放疗上有较大的优势。在放射物理学方面主要表现为有更好地剂量学优势,在对危及器官的保护上HT能更好地降低腮腺及内耳等危及器官的受照射剂量,降低了急性不良反应的发生率以不良反应程度,提高了病人的生活质量。
局部晚期鼻咽癌螺旋断层放疗与常规调强放疗的剂量学比较及近期疗效分析
Dosimetric comparison and short-term efficacy analysis of helical tomotherapy and intensity-modulated radiation therapy for locally advanced nasopharyngeal carcinoma
-
摘要:
目的通过比较局部晚期鼻咽癌在螺旋断层放疗(HT)和普通调强放疗(IMRT)两种放疗设备治疗系统下的剂量学、急性不良反应及近期疗效等方面的差异,观察HT在局部晚期鼻咽癌治疗中的剂量学优势、近期疗效及不良反应。 方法回顾性分析2017年2月至2019年10月局部晚期鼻咽癌140例,其中HT组70例,IMRT组70例。依据病人头颈部磁共振成像进行肿瘤的靶区勾画。鼻咽癌原发病灶处方剂量为69.96 Gy/33F,转移淋巴结的处方剂量为66~70 Gy/33F,高危区处方剂量为60 Gy/33F,低危区处方剂量为50~54 Gy/33F。2组在放疗同时均给予以顺铂为基础的同步化疗,顺铂剂量为80 mg/m2,3周为一个周期。根据RTOG/EORTC标准评价放疗的急性不良反应。根据RECTST 1.1标准进行实体瘤的疗效评价。统计分析2组治疗计划的放射物理剂量学差异、自放疗开始至放疗结束后1个月病人的近期疗效以及放化疗相关的急性不良反应。 结果在处方剂量中,HT组在靶区均匀性指数上与IMRT组差异无统计学意义(P>0.05),其余变量中HT组在靶区适形度及均匀性指数上均优于IMRT组(P < 0.05~P < 0.01)。2组病人的近期疗效相似(P>0.05)。HT组在耳鸣及急性腮腺损伤等放疗不良反应方面较IMRT组轻(P < 0.05)。 结论相比普通IMRT,HT在局部晚期鼻咽癌的放疗上具有更好的放射物理相关的剂量学优势。尽管2组近期疗效相似,但HT在急性腮腺损伤及听力损伤等方面具更低的不良反应。 Abstract:ObjectiveTo compare the dosimetry, acute adverse reactions and short-term therapeutic effects of helical tomotherapy(HT) and intensity-modulated radiation therapy(IMRT) for locally advanced nasopharyngeal carcinoma, and observe the dosimetric advantage, short-term efficacy and adverse reactions of HT in the treatment of locally advanced nasopharyngeal carcinoma. MethodsThe clinical data of 140 patients with locally advanced nasopharyngeal carcinoma from February 2017 to October 2019 were retrospectively analyzed, which included 70 patients treatment with HT and 70 patients treatment with IMRT.The target area of tumor was delineated according to the magnetic resonance imaging(MRI) of head and neck.The prescription doses of the primary nasopharyngeal carcinoma, metastatic lymph node, high-risk area and low-risk area were 69.96 Gy/33F, 66-70 Gy/33F, 60 Gy/33F and 50-54 Gy/33F, respectively.Two groups were treated with cisplatin based on concurrent chemotherapy at the same time of radiotherapy, with cisplatin dose of 80 mg/m2 for a 3-week cycle.The acute adverse reactions of radiotherapy were evaluated according to RTOG/EORTC criteria.The efficacy of solid tumors was evaluated according to RECTST 1.1 criteria.The differences of radiophysical dosimetry, short-term efficacy of patients from the beginning of radiotherapy to 1 month after the end of radiotherapy, and acute adverse reactions related to radiotherapy and chemotherapy were statistically analyzed between two groups. ResultsIn the prescribed dose, there was no statistical significance in the homogeneity index of target area between the HT group and IMRT group(P>0.05).Among other variables, the conformation number and homogeneity index of target area in HT group were better than that in IMRT group(P < 0.05 to P < 0.01).The short-term efficacy in two groups was similar(P>0.05).The tinnitus and acute parotid gland injury in HT group were less severe than that in IMRT group(P < 0.05). ConclusionsCompared with IMRT, HT has a better dosimetry advantage in radiotherapy of locally advanced nasopharyngeal carcinoma.Although the short-term efficacy is similar in both groups, HT has less adverse reactions on acute parotid injury and hearing loss. -
Key words:
- nasopharyngeal neoplasms /
- helical tomography /
- dosimetric analysis /
- adverse reaction
-
表 1 2组基线资料比较(n)
分组 n 男 女 年龄/岁 病理类型 分期/期 鳞状细胞癌 分化性非角化性癌 未分化癌 Ⅲ Ⅳa HT组 70 54 16 49.63±14.70 10 25 35 37 33 IMRT组 70 55 15 53.19±12.58 8 23 39 41 29 χ2 — 0.04 1.54* 0.52 0.46 P — >0.05 >0.05 >0.05 >0.05 *示t值 表 2 HT组与IMRT组靶区CN和HI比较
分组 n PGTVnx PGTVnd PTV1 PTV2 CN HI CN HI CN HI CN HI HT组 70 0.91±0.01 1.06±0.01 0.91±0.02 1.08±0.04 0.90±0.02 1.19±0.02 0.89±0.03 1.08±0.02 IMRT组 70 0.90±0.03 1.06±0.01 0.88±0.04 1.02±0.03 0.86±0.03 1.21±0.03 0.84±0.02 1.09±0.02 t — 2.65* 0.00 5.61* 10.04* 9.28* 4.64* 11.60* 2.96 P — <0.05 >0.05 <0.01 <0.01 <0.01 <0.01 <0.01 <0.01 *示t′值 表 3 HT组与IMRT组计划中危及器官的最大和平均剂量比较(x±s; Gy)
分组 n 眼球 晶体 视神经 视交叉 脑干 脊髓 腮腺 内耳 口腔 下颌骨 最大剂量 HT组 70 20.26±6.21 3.92±1.78 31.58±14.65 33.32±12.78 51.08±5.26 37.08±3.22 71.46±2.98 54.19±3.37 61.90±11.13 61.45±7.65 MRT组 70 22.92±7.22 4.68±0.45 32.88±7.91 34.87±16.76 54.10±2.55 41.88±2.04 74.02±2.89 56.09±2.21 67.29±9.78 63.65±5.90 t — 2.34 3.46* 0.65* 0.62* 4.32* 10.54* 5.16 3.94* 3.04 1.91 P — <0.05 <0.01 >0.05 >0.05 <0.01 <0.01 <0.01 <0.01 <0.01 >0.05 平均剂量 HT组 70 5.02±1.42 2.85±1.33 24.54±8.81 27.76±9.91 34.56±5.36 27.02±5.04 35.77±3.55 38.90±3.47 31.18±7.06 46.19±8.77 MRT组 70 6.05±2.10 4.54±0.75 26.65±7.10 28.32±12.42 37.12±6.10 30.07±2.11 39.09±2.02 47.63±3.65 39.62±6.35 43.71±6.67 t — 3.40* 9.26* 1.56 0.29 2.64 4.67* 6.80* 14.50 7.44 1.88* P — <0.05 <0.01 >0.05 >0.05 <0.01 <0.01 <0.01 <0.01 <0.01 >0.05 *示t′值 表 4 HT组与IMRT组病人不良反应比较(n)
分组 n 0级 Ⅰ级 Ⅱ级 Ⅲ级 Ⅳ级 uc P 口腔黏膜炎 140 0 29 74 36 1 0.15 >0.05 HT组 70 0 11 43 16 0 IMRT组 70 0 18 31 20 1 耳鸣 120 104 10 5 1 0 2.17 <0.05 HT组 60 56 3 1 0 0 IMRT组 60 48 7 4 1 0 腮腺损伤 140 9 73 58 0 0 4.87 <0.01 HT组 70 9 45 16 0 0 IMRT组 70 0 28 42 0 0 放射性皮炎 140 1 19 96 23 1 0.60 >0.05 HT组 70 1 8 48 12 1 IMRT组 70 0 11 48 11 0 咽喉疼痛 140 9 115 13 3 0 1.42 >0.05 HT组 70 5 60 4 1 0 IMRT组 70 4 55 9 2 0 消化系统反应 140 9 97 29 5 0 0.47 >0.05 HT组 70 4 51 12 3 0 IMRT组 70 5 46 17 2 0 白细胞减少 140 46 16 47 21 10 1.45 >0.05 HT组 70 26 9 22 10 3 IMRT组 70 20 7 25 11 7 血小板降低 140 101 27 9 3 0 0.49 >0.05 HT组 70 52 12 4 2 0 IMRT组 70 49 15 5 1 0 肝功能损伤 140 127 8 5 0 0 0.82 >0.05 HT组 70 62 6 2 0 0 IMRT组 70 65 2 3 0 0 肾功能损伤 140 135 4 1 0 0 0.49 >0.05 HT组 70 68 2 0 0 0 IMRT组 70 67 2 1 0 0 疲劳 140 7 92 41 0 0 1.04 >0.05 HT组 70 4 42 24 0 0 IMRT组 70 3 50 17 0 0 体质量减轻 122 35 55 24 8 0 0.68 >0.05 HT组 70 20 30 12 8 0 IMRT组 52 15 25 12 0 0 表 5 HT组与IMRT组病人近期疗效比较(n)
分组 n CR PR SD PD ORR/% uc P HT组 70 44 22 4 0 94.29 0.71 >0.05 IMRT组 70 40 25 4 1 92.86 合计 140 84 47 8 1 93.57 -
[1] ZHANG Y, CHEN L, HU GQ, et al. Gemcitabine and cisplatin induction chemotherapy in nasopharyngeal carcinoma[J]. N Engl J Med, 2019, 381(12): 1124. doi: 10.1056/NEJMoa1905287 [2] MAO YP, XIE FY, LIU LZ, et al. Re-evaluation of 6th edition of AJCC staging system for nasopharyngeal carcinoma and proposed improvement based on magnetic resonance imaging[J]. Int J Radiat Oncol Biol Phys, 2009, 73(5): 1326. doi: 10.1016/j.ijrobp.2008.07.062 [3] ZHANG L, HUANG Y, HONG S, et al. Gemcitabine plus cisplatin versus fluorouracil plus cisplatin in recurrent or metastatic nasopharyngeal carcinoma: a multicentre, randomised, open-label, phase 3 trial[J]. Lancet, 2016, 388(10054): 1883. doi: 10.1016/S0140-6736(16)31388-5 [4] SUN Y, LI WF, CHEN NY, et al. Induction chemotherapy plus concurrent chemoradiotherapy versus concurrent chemoradiotherapy alone in locoregion-ally advanced nasopharyngeal carcinoma: a phase 3, multicentre, randomised controlled trial[J]. Lancet Oncol, 2016, 17: 1509. doi: 10.1016/S1470-2045(16)30410-7 [5] LIN S, PAN J, HAN L, et al. Update report of nasopharyngeal carcinoma treated with reduced-volume intensity-modulated radiation therapy and hypothesis of the optimal margin[J]. Radiother Oncol, 2014, 110(3): 385. doi: 10.1016/j.radonc.2014.01.011 [6] LEE AW, NG WT, CHAN LL, et al. Evolution of treatment for nasopharyngeal cancer success and setback in the intensity-modulated radiotherapy era[J]. Radiother Oncol, 2014, 110(3): 377. doi: 10.1016/j.radonc.2014.02.003 [7] LU SH, CHENG CH, KUO SH, et al. volumetric modulated arc therapy for nasopharyngeal carcinoma: a dosimetric comparison with TomoTherapy and step-and shoot IMRT[J]. Radiother Oncol, 2012, 104(3): 324. doi: 10.1016/j.radonc.2011.11.017 [8] DU L, ZHANG XX, MA L, et al. Clinical study of nasopharyngeal carcinoma treated by helical tomotherapy in China: 5-year outcomes[J]. Biomed Res Int, 2014, 2014: 980767. [9] HERRMANN T, KNORR A, DRNER K. The RTOG/EORTC classification criteria for early and late radiation reactions[J]. Radiobiol Radiother(Berl), 1987, 28(4): 519. [10] EISENHAUER EA, THERASSE P, BOGAERTS J, et al. New response evaluation criteriain solid tumours: revised RECIST guideline(version 1.1)[J]. Eur J Cancer, 2009, 45(2): 228. doi: 10.1016/j.ejca.2008.10.026 [11] PUEBLA F, LOPEZ GUERRA JL, GARCIA RAMIREZ JM, et al. Effectiveness and toxicity of helical tomotherapy for patients with locally recurrent nasopharyngeal carcinoma[J]. Clin Transl Oncol, 2015, 17(11): 925. doi: 10.1007/s12094-015-1328-5 [12] ZHANG X, DU L, ZHAO FF, et al. A phase Ⅱ clinical trial of concurrent helical tomotherapy plus cetuximab filllowed by adjuvant chemotherapy with cisplatin and docetaxel for locally advanced nasopharyngeal eareiuolna[J]. Int J Biol Sci, 2016, 12(4): 446. doi: 10.7150/ijbs.12937 [13] 周闪, 钱建军, 徐亮, 等. 涎腺早期放射性损伤的磁共振定量评价[J]. 中华医学杂志, 2017, 97(7): 492. doi: 10.3760/cma.j.issn.0376-2491.2017.07.004 [14] LU SH, CHENG JC, KUO SH, et al. Volumetric modulated arc therapy for nasopharyngeal carcinoma: a dosimetric comparison with Tomo Therapy and step-and-shoot IMRT[J]. Radiother Oncol, 2012, 104(3): 324. doi: 10.1016/j.radonc.2011.11.017 [15] SERVAGI VERNAT S, ALI D, PUYRAVEAU M, et al. Is IMAT the ultimate evolution of conformal radiotherapy? Dosimetric comparison of helical tomotherapy and volumetric modulated arc therapy for oropharyngeal cancer in a planning study[J]. Phys Med, 2014, 30(3): 280. doi: 10.1016/j.ejmp.2013.07.128 [16] LEUNG SW, LEE TF. Treatment of nasopharyngeal carcinoma bytomotherapy: five-year experience[J]. Radiat Oncol, 2013, 8(1): 107. doi: 10.1186/1748-717X-8-107 [17] LU J, MA YD, CHEN JH, et al. Assessment of anatomical and Dosimetric changes by a deformable registration method during the course of intensity-modulated radiotherapy for nasopharyngeal carcinoma[J]. J Radiat Res, 2014, 55(1): 97. doi: 10.1093/jrr/rrt076 [18] DUMA M N, KAMPFER S, WILKENS JJ, et al. Comparative analysis of an image-guided versus a non-image-guided setup approach in terms of delivered dose to the parotid glands in head-and-neck cancer IMRT[J]. Int J Radiat Oncol Biol Phys, 2010, 77(4): 1266. doi: 10.1016/j.ijrobp.2009.09.047 [19] BHANDARE N, JACKSON A, EISBRUEH A, et al. Radiation therapy and hearing loss[J]. Int J Radiat Oncol Biol Phys, 2010, 76(3): 50. doi: 10.1016/j.ijrobp.2009.04.096 [20] 卢丽娜, 钱建军, 宦坚, 等. 鼻咽癌IMRT中耳蜗限量和内耳整体限量方法对内耳结构保护差异的研究[J]. 中华放射肿瘤学杂志, 2017, 26(9): 997. doi: 10.3760/cma.j.issn.1004-4221.2017.09.004 [21] LI JX, ZHAO ZF, WU X, et al. Bevacizumab plus cisplatin and helical tomotherapy in treatment of locally advanced nasopharyngeal carcinoma[J]. Onco Targets Ther, 2015(8): 1315. -




 下载:
下载: