-
结肠癌是世界上最高发的恶性肿瘤之一,尽管外科手术治疗取得一定进展,但其死亡率一直居高不下,对于晚期及转移性结肠癌,多学科的综合治疗是其重要手段,其中靶向治疗越来越受到关注[1-3]。研究[4]表明circRNA参与调控结肠癌的进展,可作为潜在的生物标志物,为结肠癌提供潜在的治疗靶点。circ_0000515位于chr14:20811305-20811534,又名circRPPH1,circ_0000515低表达与宫颈癌病人预后良好相关;circ_0000515充当miR-326海绵通过上调ELK1促进宫颈癌的进展[5]。circRPPH1在体内促进乳腺癌细胞的增殖、迁移、侵袭和血管生成以及肿瘤生长[6]。然而circ_0000515对结肠癌细胞增殖和凋亡的影响及机制尚不清楚。研究[7-8]报道上调的miR-1258可抑制结直肠癌细胞的增殖和迁移。miR-1258上调显著抑制骨肉瘤细胞增殖,并促进细胞周期停滞在G0/G1[9]。circ_0101432通过靶向miR-1258和miR-622并上调MAPK1表达来抑制肝癌细胞凋亡,促进细胞增殖,侵袭能力和肿瘤生长[10]。然而circ_0000515是否通过调控miR-1258影响结肠癌细胞增殖和凋亡尚不清楚。
-
选取我院病理科存档且已确诊的结肠癌病人癌组织及癌旁组织标本41例,其中男24例,女17例,年龄33~75岁,平均(39.9±1.1)岁;所有病人均知情且同意。
-
结肠癌细胞株SW620购自美国ATCC;RPMI-1640培养基购自美国Gibco公司;Trizol试剂和荧光定量PCR试剂盒购自日本Takara公司;MTT试剂盒、Annexin V-FITC/PI凋亡检测试剂盒购自日本同仁研究所;蛋白提取试剂盒购自上海碧云天生物有限公司;双荧光素酶报告基因检测试剂盒购自上海沪震实业有限公司。
-
结肠癌细胞株SW620用RPMI-1640培养基常规培养,将circ_0000515干扰表达载体及其阴性对照、miR-1258模拟物及其阴性对照转染至SW620细胞中,记为si-circ_0000515组、si-NC组、miR-1258组、miR-NC组;将circ_0000515干扰表达载体分别与miR-1258抑制剂及其阴性对照转染至SW620细胞中,记为si-circ_0000515+anti-miR-1258组、si-circ_0000515+anti-miR-NC组。
-
提取结肠癌组织及细胞总RNA,按试剂盒使用说明进行RT-qPCR,PCR反应条件:95 ℃预变性3 min,95 ℃变性30 s,60 ℃退火30 s,72 ℃延伸30 s,共40个循环;融解曲线:95 ℃ 15 s,60 ℃ 15 s,95 ℃ 15 s。相对表达量用2-△△Ct法计算。
-
细胞培养48 h,按试剂盒说明操作,用酶标仪于450 nm处检测吸光度(OD)值。
-
收集培养48 h细胞,按试剂盒说明书操作,上流式细胞仪检测。
-
收集细胞,提取总蛋白,取50 μL样品进行SDS-PAGE,电转至PVDF,封闭后加入一抗,4 ℃过夜,加入二抗室温1 h,显影、定影,成像后检测蛋白条带灰度水平,以GAPDH为内参计算蛋白表达水平。
-
构建circ_0000515的野生型和突变型荧光素酶载体WT-circ_0000515和MUT-circ_0000515,将其分别与miR-NC和miR-1258共转染至SW620细胞中,按照说明书检测荧光素酶活性。
将circ_0000515干扰表达载体、过表达载体及其阴性对照转染至SW620细胞中,按1.4中方法检测miR-1258表达水平。
-
采用两独立样本t(或t′)检验、配对t检验、单因素方差分析和q检验。
-
与癌旁组织比较,结肠癌组织中circ_0000515表达水平升高,miR-1258表达水平降低,差异均有统计学意义(P < 0.01)(见表 1)。
分组 n circ_0000515 miR-1258 癌旁组织 41 1.00±0.07 1.00±0.07 结肠癌组织 41 3.90±0.24 0.33±0.03 t — 78.17 67.49 P — < 0.01 < 0.01 表 1 circ_0000515和miR-1258在结肠癌组织中的表达(x±s)
-
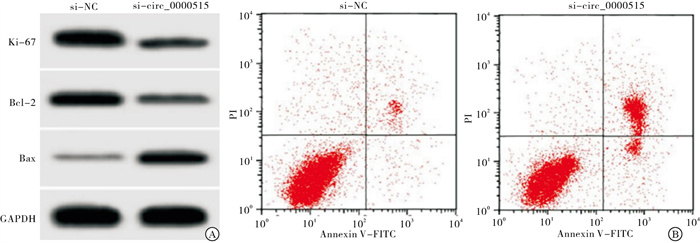
与si-NC组比较,si-circ_0000515组circ_0000515表达水平降低,SW620细胞活性降低,SW620细胞的凋亡率升高,SW620细胞中Ki-67、Bcl-2表达水平降低,Bax表达水平升高,差异均有统计学意义(P < 0.01)(见图 1、表 2)。
分组 n circ_0000515 OD值(450 nm) 凋亡率/% Ki-67蛋白 Bcl-2蛋白 Bax蛋白 si-NC 9 1.00±0.07 0.84±0.06 7.16±0.65 0.72±0.05 0.61±0.04 0.16±0.02 si-circ_0000515 9 0.36±0.03 0.48±0.04 25.90±2.08 0.32±0.03 0.26±0.03 0.59±0.04 t — 25.21* 14.98 25.80* 20.58 21.00 28.85 P — < 0.01 < 0.01 < 0.01 < 0.01 < 0.01 < 0.01 *示t′值 表 2 抑制circ_0000515表达对结肠癌SW620细胞增殖和凋亡的影响(x±s)
-
Circular RNA Interactome预测显示circ_0000515的序列中含有与miR-1258互补的核苷酸序列(见图 2);miR-1258与WT-circ_0000515共转染的SW620细胞荧光素酶活性降低,差异有统计学意义(P < 0.01),而与MUT-circ_0000515共转染的SW620细胞荧光素酶活性差异无统计学意义(P>0.05)(见表 3)。过表达circ_0000515后miR-1258表达水平降低,抑制circ_0000515表达后miR-1258表达水平升高,差异均有统计学意义(P < 0.05)(见表 4)。
分组 n WT-circ_0000515 MUT-circ_0000515 miR-NC 9 0.99±0.05 0.97±0.06 miR-1258 9 0.42±0.04 1.00±0.07 t — 26.71 0.98 P — < 0.01 >0.05 表 3 双荧光素酶报告实验(x±s)
分组 n miR-1258 pcDNA 9 1.00±0.06 pcDNA-circ_0000515 9 0.33±0.03* si-NC 9 0.99±0.06 si-circ_0000515 9 2.74±0.21# F — 734.64 P — < 0.01 MS组内 — 0.013 q检验:与pcDNA组比较*P < 0.05;与si-NC组比较#P < 0.05 表 4 circ_0000515调控miR-1258的表达(x±s)
-
与miR-NC组比较,miR-1258组miR-1258表达水平升高,SW620细胞活性降低,SW620细胞的凋亡率升高,SW620细胞中Ki-67、Bcl-2表达水平降低,Bax表达水平升高,差异均有统计学意义(P < 0.01)(见图 3、表 5)。
分组 n miR-1258 OD值(450 nm) 凋亡率/% Ki-67蛋白 Bcl-2蛋白 Bax蛋白 miR-NC 9 1.00±0.06 0.87±0.05 6.87±0.55 0.74±0.05 0.64±0.05 0.13±0.02 miR-1258 9 3.40±0.29 0.53±0.04 19.98±1.89 0.39±0.03 0.33±0.03 0.52±0.04 t — 24.31* 15.93 19.98* 18.01 15.95 26.16 P — < 0.01 < 0.01 < 0.01 < 0.01 < 0.01 < 0.01 *示t′值 表 5 过表达miR-1258对结肠癌SW620细胞增殖和凋亡的影响(x±s)
-
与si-circ_0000515+anti-miR-NC组比较,si-circ_0000515+anti-miR-1258组miR-1258表达水平降低,SW620细胞活性升高,SW620细胞的凋亡率降低,SW620细胞中Ki-67、Bcl-2表达水平升高,Bax表达水平降低,差异均有统计学意义(P < 0.01)(见图 4、表 6)。
分组 n miR-1258 OD值(450 nm) 凋亡率/% Ki-67蛋白 Bcl-2蛋白 Bax蛋白 si-circ_0000515+anti-miR-NC 9 1.00±0.05 0.46±0.04 27.35±2.23 0.30±0.02 0.25±0.02 0.60±0.04 si-circ_0000515+anti-miR-1258 9 0.29±0.03 0.73±0.06 11.84±1.17 0.64±0.05 0.48±0.04 0.27±0.02 t — 36.53 11.23 18.48 18.94 15.43 22.14 P — < 0.01 < 0.01 < 0.01 < 0.01 < 0.01 < 0.01 表 6 干扰miR-1258表达逆转了抑制circ_0000515表达对结肠癌SW620细胞增殖和凋亡的作用(x±s)
-
分子靶向治疗作为新型癌症治疗方法,其在结肠癌的治疗中也具有重要意义,而寻找可靠的分子靶点是实现靶向药物治疗的关键[11-12]。研究[13]报道circ_0000515在肝癌组织和细胞系中上调,可用于预测肝癌的肿瘤分期,淋巴转移和预后;敲除circ_0000515可减弱肝癌Hep3B和MHCC88H细胞的增殖和迁移能力。circ_0000515通过调控miR-296-5p/CXCL10轴促进乳腺癌细胞的增殖和侵袭[14]。circ_0000515在肿瘤中可能起促癌作用。本实验结果显示,结肠癌组织中circ_0000515表达水平升高;抑制circ_0000515表达后,SW620细胞活性降低,SW620细胞的凋亡率升高,SW620细胞中Ki-67、Bcl-2表达水平降低,Bax表达水平升高;说明抑制circ_0000515表达可抑制结肠癌细胞增殖、促进细胞凋亡。
研究[15]报道miR-1258通过GRB2/Ras/Erk途径抑制非小细胞肺癌细胞增殖并诱导衰老和凋亡。miR-1258的过表达抑制了甲状腺乳头状癌KTC-1细胞的活力以及迁移和侵袭的能力[16]。本实验结果显示,结肠癌组织中miR-1258表达水平降低;过表达miR-1258抑制SW620细胞增殖,促进细胞凋亡。研究发现circ_0046599可以通过使miR-1258海绵化而增加RPN2表达来促进肝细胞癌的发展[17]。circ_002178通过调节miR-1258/KDM7A轴来促进乳腺癌细胞的生长和迁移[18]。说明circRNA可通过调控miR-1258影响肿瘤进展。本实验结果显示,circ_0000515靶向调控miR-1258;干扰miR-1258表达逆转了抑制circ_0000515表达对结肠癌SW620细胞增殖和凋亡的作用。
综上所述,抑制circ_0000515表达通过靶向上调miR-1258抑制结肠癌细胞增殖,促进凋亡。
circ_0000515靶向miR-1258调控结肠癌细胞增殖和凋亡的机制研究
Effect of circ_0000515 targeting miR-1258 on the proliferation and apoptosis in the colon cancer cells
-
摘要:
目的探讨circ_0000515调控结肠癌细胞增殖和凋亡的分子机制。 方法选取41例结肠癌病人癌组织及癌旁组织标本,用实时荧光定量PCR(RT-qPCR)检测circ_0000515和miR-1258的表达水平;结肠癌细胞SW620分为si-circ_0000515组、si-NC组、miR-1258组、miR-NC组、si-circ_0000515+anti-miR-NC组、si-circ_0000515+anti-miR-1258组。四甲基偶氮唑盐比色法(MTT)检测SW620细胞活性;流式细胞术检测SW620细胞凋亡;双荧光素酶报告实验检测circ_0000515和miR-1258的靶向关系。 结果与癌旁组织比较,结肠癌组织中circ_0000515表达水平升高,miR-1258表达水平降低(P < 0.01)。抑制circ_0000515表达或过表达miR-1258,SW620细胞活性降低,SW620细胞的凋亡率升高(P < 0.01)。circ_0000515靶向调控miR-1258;干扰miR-1258表达逆转了抑制circ_0000515表达对结肠癌SW620细胞增殖和凋亡的作用。 结论抑制circ_0000515表达通过靶向上调miR-1258抑制结肠癌细胞增殖,促进凋亡。 -
关键词:
- 结肠肿瘤 /
- circ_0000515 /
- miR-1258 /
- 增殖 /
- 凋亡
Abstract:ObjectiveTo explore the molecular mechanism of circ_0000515 regulating the proliferation and apoptosis of colon cancer cells. MethodsA total of 41 cases of colon cancer patients with cancer tissue and adjacent tissue samples were selected.Real-time fluorescent quantitative PCR was used to detect the expression of circ_0000515 and miR-1258.Colon cancer cells SW620 were divided into si-circ_0000515 group, si-NC group, miR-1258 group, miR-NC group, si-circ_0000515+anti-miR-NC group, si-circ_0000515+anti-miR-1258 group.Tetramethylazolium salt colorimetric assay(MTT) was used to detect the cell viability.Flow cytometry was used to detect apoptosis.The targeting relationship of circ_0000515 and miR-1258 was detected by dual-luciferase reporter assay. ResultsCompared with the adjacent tissues, the expression of circ_0000515 in colon cancer tissues was increased, and the expression of miR-1258 was decreased(P < 0.01).After the inhibition of circ_0000515 expression or overexpression of miR-1258, the viability of SW620 cells was decreased, the apoptosis rate was increased(P < 0.01).Circ_0000515 targeted and regulated the expression of miR-1258.Interference with miR-1258 expression reversed the effect of inhibiting circ_0000515 expression on the proliferation and apoptosis of colon cancer SW620 cells. ConclusionsInhibiting the expression of circ_0000515 by up-regulation of miR-1258 can inhibit the proliferation and promote the apoptosis in colon cancer cells. -
Key words:
- colon neoplasms /
- circ_0000515 /
- miR-1258 /
- proliferation /
- apoptosis
-
表 1 circ_0000515和miR-1258在结肠癌组织中的表达(x±s)
分组 n circ_0000515 miR-1258 癌旁组织 41 1.00±0.07 1.00±0.07 结肠癌组织 41 3.90±0.24 0.33±0.03 t — 78.17 67.49 P — < 0.01 < 0.01 表 2 抑制circ_0000515表达对结肠癌SW620细胞增殖和凋亡的影响(x±s)
分组 n circ_0000515 OD值(450 nm) 凋亡率/% Ki-67蛋白 Bcl-2蛋白 Bax蛋白 si-NC 9 1.00±0.07 0.84±0.06 7.16±0.65 0.72±0.05 0.61±0.04 0.16±0.02 si-circ_0000515 9 0.36±0.03 0.48±0.04 25.90±2.08 0.32±0.03 0.26±0.03 0.59±0.04 t — 25.21* 14.98 25.80* 20.58 21.00 28.85 P — < 0.01 < 0.01 < 0.01 < 0.01 < 0.01 < 0.01 *示t′值 表 3 双荧光素酶报告实验(x±s)
分组 n WT-circ_0000515 MUT-circ_0000515 miR-NC 9 0.99±0.05 0.97±0.06 miR-1258 9 0.42±0.04 1.00±0.07 t — 26.71 0.98 P — < 0.01 >0.05 表 4 circ_0000515调控miR-1258的表达(x±s)
分组 n miR-1258 pcDNA 9 1.00±0.06 pcDNA-circ_0000515 9 0.33±0.03* si-NC 9 0.99±0.06 si-circ_0000515 9 2.74±0.21# F — 734.64 P — < 0.01 MS组内 — 0.013 q检验:与pcDNA组比较*P < 0.05;与si-NC组比较#P < 0.05 表 5 过表达miR-1258对结肠癌SW620细胞增殖和凋亡的影响(x±s)
分组 n miR-1258 OD值(450 nm) 凋亡率/% Ki-67蛋白 Bcl-2蛋白 Bax蛋白 miR-NC 9 1.00±0.06 0.87±0.05 6.87±0.55 0.74±0.05 0.64±0.05 0.13±0.02 miR-1258 9 3.40±0.29 0.53±0.04 19.98±1.89 0.39±0.03 0.33±0.03 0.52±0.04 t — 24.31* 15.93 19.98* 18.01 15.95 26.16 P — < 0.01 < 0.01 < 0.01 < 0.01 < 0.01 < 0.01 *示t′值 表 6 干扰miR-1258表达逆转了抑制circ_0000515表达对结肠癌SW620细胞增殖和凋亡的作用(x±s)
分组 n miR-1258 OD值(450 nm) 凋亡率/% Ki-67蛋白 Bcl-2蛋白 Bax蛋白 si-circ_0000515+anti-miR-NC 9 1.00±0.05 0.46±0.04 27.35±2.23 0.30±0.02 0.25±0.02 0.60±0.04 si-circ_0000515+anti-miR-1258 9 0.29±0.03 0.73±0.06 11.84±1.17 0.64±0.05 0.48±0.04 0.27±0.02 t — 36.53 11.23 18.48 18.94 15.43 22.14 P — < 0.01 < 0.01 < 0.01 < 0.01 < 0.01 < 0.01 -
[1] 王嘉源, 董卫国. 结肠癌靶向治疗研究[J]. 胃肠病学和肝病学杂志, 2020, 29(7): 721. doi: 10.3969/j.issn.1006-5709.2020.07.001 [2] 杨波, 张艳君, 彭海生, 等. 结肠癌及其分型的靶分子修饰递送药物的研究进展[J]. 中国药房, 2019, 30(18): 2577. [3] ZYKOVA T, ZHU F, WANG L, et al. Targeting PRPK function blocks colon cancer metastasis[J]. Mol Cancer Ther, 2018, 17(5): 1101. doi: 10.1158/1535-7163.MCT-17-0628 [4] 陈佳权, 陈典, 方喜平. 环状RNA circ_100290在结直肠癌中的表达及其临床意义[J]. 蚌埠医学院学报, 2019, 44(10): 20. [5] TANG Q, CHEN Z, ZHAO L, et al. Circular RNA hsa_circ_0000515 acts as a miR-326 sponge to promote cervical cancer progression through up-regulation of ELK1[J]. Aging, 2019, 11(22): 9982. doi: 10.18632/aging.102356 [6] ZHOU Y, LIU X, LAN J, et al. Circular RNA circRPPH1 promotes triple-negative breast cancer progression via the miR-556-5p/YAP1 axis[J]. Am J Transl Res, 2020, 12(10): 6220. [7] ZHANG Z, LI J, HUANG Y, et al. Upregulated miR-1258 regulates cell cycle and inhibits cell proliferation by directly targeting E2F8 in CRC[J]. Cell Prolif, 2018, 51(6): e12505. doi: 10.1111/cpr.12505 [8] HWANG JS, JEONG EJ, CHOI J, et al. MicroRNA-1258 inhibits the proliferation and migration of human colorectal cancer cells through suppressing CKS1B expression[J]. Genes, 2019, 10(11): 912. doi: 10.3390/genes10110912 [9] LIU W, ZHOU Z, ZHANG Q, et al. Overexpression of miR-1258 inhibits cell proliferation by targeting AKT3 in osteosarcoma[J]. Biochem Biophys Res Commun, 2019, 510(3): 479. doi: 10.1016/j.bbrc.2019.01.139 [10] ZOU H, XU X, LUO L, et al. Hsa_circ_0101432 promotes the development of hepatocellular carcinoma(HCC) by adsorbing miR-1258 and miR-622[J]. Cell Cycle, 2019, 18(19): 2398. doi: 10.1080/15384101.2019.1618120 [11] 杜飞, 董亚萍, 朴成钢. 结肠癌靶向治疗的研究进展[J]. 生命的化学, 2018, 38(2): 259. [12] 丁志海. 靶向药物治疗转移性结肠癌的研究进展[J]. 医疗装备, 2018, 31(6): 203. doi: 10.3969/j.issn.1002-2376.2018.06.152 [13] LI H, LI CM, YUAN R, et al. Circ_0000515 drives the progression of hepatocellular carcinoma by regulating MAPK10[J]. Eur Rev Med Pharmacol Sci, 2020, 24(11): 6014. [14] CAI F, FU W, TANG L, et al. Hsa_circ_0000515 is a novel circular RNA implicated in the development of breast cancer through its regulation of the microRNA-296-5p/CXCL10 axis[J]. FEBS J, 2020, 288(3): 861. [15] JIANG W, WEI K, PAN C, et al. MicroRNA-1258 suppresses tumour progression via GRB2/Ras/Erk pathway in non-small-cell lung cancer[J]. Cell Prolif, 2018, 51(6): e12502. doi: 10.1111/cpr.12502 [16] WANG LJ, CAI HQ. miR-1258: a novel microRNA that controls TMPRSS4 expression is associated with malignant progression of papillary thyroid carcinoma[J]. Endokrynol Pol, 2020, 71(2): 146. doi: 10.5603/EP.a2020.0009 [17] FANG Q, LIU H, ZHOU A, et al. Circ_0046599 promotes the development of hepatocellular carcinoma by regulating the miR-1258/RPN2 network[J]. Cancer Manag Res, 2020, 12: 6849. doi: 10.2147/CMAR.S253510 [18] LI W, YANG X, SHI C, et al. Hsa_circ_002178 promotes the growth and migration of breast cancer cells and maintains cancer stem-like cell properties through regulating miR-1258/KDM7A axis[J]. Cell Transplant, 2020, 29: 963689720960174. -





 下载:
下载: