-
糖尿病病人心血管并发症之一为糖尿病心肌病(diabetic cardiomyopathy,DCM),DCM是危险且常见的并发症,其重要的病理生理学特征改变是心肌细胞原发性损伤会引起结构异常而导致心肌纤维化[1]。研究[2]显示,Wnt信号通路在心脏发育与血管生成过程中承担重要调控作用。Wnt信号通路在心脏发育早期被激活,加速心脏祖细胞的增殖和迁移,但其活性在心脏发育晚期则被抑制,促进心肌细胞分化[3]。因此,阻断Wnt信号通路的异常激活可以在临床上用作糖尿病心肌纤维化干预及治疗的方法[4]。
药材丹参首次被记录在《神农本草经》里,并在上品之列,它含有众多化学成分,其中酚酸类物质是主要水溶性成分,为丹参抗心血管疾病的主要活性物质。酚酸类化合物具有加强心肌收缩能力、调节心脏功能、平衡心肌耗氧量;扩张冠状动脉, 增加血流量;防止血小板聚集、抗血栓形成, 并影响血液流变学;改善肝脏微循环、降低血脂等效果[5-6]。丹参作为活血化瘀之要药在中医药领域广泛使用,但其主要有效成分丹酚酸A作用于心肌纤维化的效果研究不多见。本研究使用由高浓度葡萄糖诱导心肌成纤维细胞体外培养模型,观察丹酚酸A对心肌成纤维细胞中Wnt信号传导途径的调节。
-
SPF级SD大鼠,出生24 h内,雌雄不限(北京维通利华实验动物技术有限公司,许可证号11400700012085、11400700016098)。
-
标准品丹酚酸A(沈阳药科大学中药化学实验室赠送);卡托普利对照品(中国食品药品检定研究院);美国西格玛公司进口分装Ⅱ型胶原酶、胰蛋白酶及四氮唑盐(MTT);美国贝克曼库尔特公司DNA PREP试剂盒;美国USCN公司Ⅰ型胶原、Ⅲ型胶原ELISA试剂盒;美国RD公司TGF-β1 ELISA试剂盒;Biogenes公司的小鼠抗结蛋白单克隆抗体和小鼠抗波形蛋白单克隆抗体;智杰方远科技有限公司PVDF膜;Thermo Fisher Scientific公司的ECL发光液;美国Gibco公司DMEM高糖培养基、DMEM低糖培养基及胎牛血清(FBS);美国Abcam公司兔抗大鼠-catenin单克隆抗体、兔抗大鼠-GSK-3β单克隆抗体及兔抗大鼠p-GSK-3β单克隆抗体、兔抗大鼠GAPDH多克隆抗体和羊抗兔IgG多克隆抗体。美国BD流式细胞分析仪;美国BioTek酶联免疫分析仪;美国Bio-Rad化学发光成像系统。
-
采用差速贴壁法,根据SREEJIT等[7]方法改进,在无菌条件下快速剪开在24 h内出生的SD大鼠乳鼠胸腔,浸泡在4 ℃ 0.01% 磷酸盐缓冲液(PBS)中以除去血细胞,75%乙醇冲洗30 s后剪碎至大小1 mm3,弃掉PBS,加等体积的0.125% 胰蛋白酶和0.1% Ⅱ型胶原酶混合液,37 ℃水浴振动并消化10 min,待组织块完全消失,收集每次细胞消化悬液并用10% FBS的DMEM低糖培养液终止消化,2 000 r/min离心10 min,收集消化悬液后倾去上清,加10% FBS的DMEM低糖培养基轻轻吹打,制成细胞悬液接种在培养瓶中,37 ℃、5% CO2培养箱内培养。鉴于心肌细胞和成纤维细胞贴壁时间的差异,60 min时将上清倾去,贴壁者则为CFs,加10% FBS的DMEM低糖培养基以继续培养。待培养细胞80%~90%融合,0.25%胰酶继续消化传代(1∶2),选取2~4代细胞进行后续实验。
-
正常对照组,DMEM低糖培养基(含5.5 mmol/L D-葡萄糖);西药对照组,22 mg/L卡托普利;高渗对照组,DMEM培养基(含5.5 mmol/L D-葡萄糖+19.5 mmol/L甘露醇);模型对照组,DMEM高糖培养基(含25 mmol/L D-葡萄糖);丹酚酸A+高糖组,25、50、100 mg/L丹酚酸A+DMEM高糖培养基(含25 mmol/L D-葡萄糖)。
-
将对数期生长的CFs制备细胞悬液,以每孔100 μL、密度5×104个/毫升接种到96孔板,培养箱设置为37 ℃,5% CO2孵育24 h无血清DMEM同步化培育24 h,根据实验分组处理再孵育24、48 h,每孔滴10 μL MTT溶液,继续孵育4 h,弃掉上清,每孔加入100 μL DMSO,用酶标仪在490 nm波长下测吸光度值(OD)。
-
将CFs细胞悬液,以每孔2 mL、密度1×105个细胞/毫升接种到6孔板中,并在37 ℃、5% CO2培养箱中孵育24 h,用无血清DMEM重新同步24 h,根据实验分组处理再孵育48 h。0.25%胰蛋白酶消化成单细胞悬液,密度调整为1×106个细胞/毫升,严格按细胞DNA PREP周期试剂盒进行操作,上机进行流式细胞术的检测操作,并用MCYCLE软件进行细胞周期分析。
-
取1×105个细胞/毫升密度的CFs细胞悬液,每孔2 mL接种在6孔板中,37 ℃、5% CO2培养箱中培养24 h,无血清DMEM替换并同步化24 h,根据实验分组处理,培养48 h后分别收集细胞上清液,严格按照试剂盒说明书测定Ⅰ型胶原、Ⅲ型胶原含量,测量450 nm处OD,并根据浓度曲线计算每孔细胞浓度。
-
制成的CFs细胞悬液,测定方法按Ⅰ型胶原、Ⅲ型胶原含量的方法处理,培养48 h后分别吸出细胞上清液,严格按照试剂盒说明书测定TGF-β1的含量,测量450 nm处OD,并根据浓度曲线计算每孔细胞浓度。
-
细胞总蛋白的提取:蛋白裂解液加入到分组处理培养后的CFs中,置于冰浴上30 min,裂解物用细胞刮刀取下,2 000 r/min离心30 min取上清液,蛋白含量于紫外分光光度仪测定,样本浓度根据标准曲线计算,调节浓度后,加上样缓冲液,将蛋白煮沸3 min变性并储存在于-80 ℃冰箱中。蛋白进行SDS-聚丙烯酰胺凝胶电泳:将通过电泳分离的蛋白转移到PVDF膜上并浸于含有5%牛血清白蛋白的TBST室温封闭液中30 min,再加一抗(1∶500)孵育20 min,4 ℃冰箱中过夜。复温后将膜洗涤重复5次,10分钟/次,封闭30 min,并用二抗封闭90 min,将膜洗涤重复5次,10分钟/次,滴加ECL发光液,成像分析系统中保存采集曝光图像。应用IMAGE J软件分析各样本灰度值,蛋白相对含量为各样本和相应内参灰度比值。
-
采用t检验、方差分析和q检验。
-
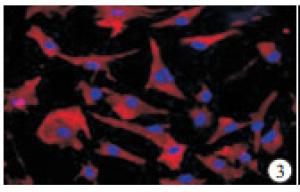
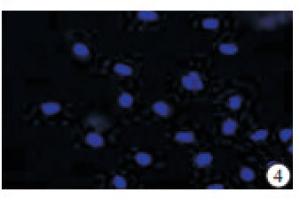
SD大鼠乳鼠心肌CFs在2~3 d会迅速生长成为融合状态。细胞体大,多为细胞质透明的梭形,具有一个卵圆形的核,通常含有1~2个核仁(见图 1、2),无自发性搏动。细胞台盼兰染色后细胞存活率>90%,经免疫组织化学染色鉴定Vinentin染色呈阳性,抗原呈红色(见图 3);Desmin染色呈阴性(见图 4)者为实验需要的CFs,细胞纯度为98%。
-
在高浓度葡萄糖条件下培养24、48 h,细胞的增殖活性均高于正常对照组(P < 0.01和P < 0.05)(见表 1)。高渗对照组细胞增殖活性与正常对照组差异无统计学意义(P>0.05),高浓度葡萄糖可以诱导CFs增殖(P < 0.01)。干预24 h后,高浓度葡萄糖可以诱导心肌成纤维细胞明显增殖(P < 0.01);与模型对照组相比,用药组均可明显抑制细胞增殖(P < 0.01),以西药对照组作用效果最明显(P < 0.01)。干预48 h后,高浓度葡萄糖可以诱导心肌成纤维细胞明显增殖(P < 0.01);与模型对照组相比,用药组均可明显抑制细胞增殖(P < 0.01),西药对照组作用效果最明显(P < 0.01)(见表 2)。
分组 OD 24 h 48 h 正常对照组 0.118±0.006 0.142±0.018 模型对照组 0.138±0.010 0.166±0.015 t 4.20 2.51 P < 0.01 < 0.05 表 1 高浓度葡萄糖在不同时间点对CFs增殖活性的作用(ni=6;x±s)
分组 OD 24 h 48 h 正常对照组 0.118±0.006 0.142±0.018 模型对照组 0.138±0.010## 0.166±0.015## 高渗对照组 0.129±0.013 0.150±0.016 100 mg/L丹酚酸A组 0.102±0.002##** 0.114±0.012** 50 mg/L丹酚酸A组 0.118±0.006**▲▲ 0.119±0.008##** 25 mg/L丹酚酸A组 0.126±0.009#**▲▲ 0.131±0.008##**▲ 西药对照组 0.080±0.003##**▲▲■■△△ 0.068±0.002##**▲▲■ ■△△ F 36.25 38.88 P < 0.01 < 0.01 MS组内 0.000 0.000 q检验:与正常对照组比较#P < 0.05,##P < 0.01;与模型对照组比较**P < 0.01;与100 mg/L丹酚酸A组比较▲P < 0.05,▲▲P < 0.01;与50 mg/L丹酚酸A组比较■■P < 0.01;与25 mg/L丹酚酸A组比较△△P < 0.01 表 2 丹酚酸A对CFs在高浓度葡萄糖培养下细胞增殖的影响(ni=6;x±s)
-
与正常对照组相比,高浓度葡萄糖可以明显降低G0+G1期CFs数量百分比(P < 0.01),明显增加S+G2+M期CFs数量百分比(P < 0.01)。与模型对照组相比,用药组能明显增加G0+G1期CFs数量百分比(P < 0.01),同时降低S+G2+M期CFs数量百分比(P < 0.01),且100 mg/L丹酚酸A的作用明显优于50 mg/L丹酚酸A(P < 0.01)(见图 5、表 3)。
分组 细胞周期(G0+G1)/% 细胞周期(S+G2+M)/% 正常对照组 97.131±0.530 2.869±0.530 模型对照组 88.987±0.929## 11.013±0.929## 100 mg/L丹酚酸A组 96.628±0.035** 3.372±0.035** 50 mg/L丹酚酸A组 92.533±0.728##**▲▲ 7.467±0.728##**▲▲ F 104.74 104.71 P < 0.01 < 0.01 MS组内 0.419 0.419 q检验:与正常对照组比较##P < 0.01;与模型对照组比较**P < 0.01;与100 mg/L丹酚酸A组比较▲▲P < 0.01 表 3 丹酚酸A对CFs在高浓度葡萄糖培养下细胞增殖周期的影响(ni=6;x±s)
-
与正常对照组相比,高浓度葡萄糖可以明显诱导CFs分泌Ⅰ型胶原、Ⅲ型胶原(P < 0.01)。与模型对照组相比,丹酚酸A各浓度组均能抑制CFs Ⅰ型胶原和Ⅲ型胶原的分泌(P < 0.05~P < 0.01),西药对照组对Ⅰ型胶原、Ⅲ型胶原分泌没有明显影响(P>0.05)(见表 4)。
分组 Ⅰ型胶原/(pg/mL) Ⅲ型胶原/(ng/mL) 正常对照组 628.11±126.89 5.31±0.24 模型对照组 2 081.69±525.70## 10.00±0.96## 100 mg/L丹酚酸A组 1 359.87±59.15##** 6.18±1.48##** 50 mg/L丹酚酸A组 1 361.94±145.35##** 6.87±2.61** 25 mg/L丹酚酸A组 1 624.49±38.06##* 6.95±1.44** 西药对照组 1 834.19±168.65##▲■ 10.12±1.12##▲▲■ ■△△ F 17.46 9.37 P < 0.01 < 0.01 MS组内 57 829.716 2.217 q检验:与正常对照组比较##P < 0.01;与模型对照组比较*P < 0.05,**P < 0.01;与100 mg/L丹酚酸A组比较▲P < 0.05,▲▲P < 0.01;与50 mg/L丹酚酸A组比较■P < 0.05,■■P < 0.01;与25 mg/L丹酚酸A组比较△△P < 0.01 表 4 丹酚酸A对CFs在高浓度葡萄糖培养下Ⅰ型胶原、Ⅲ型胶原分泌的影响(ni=6;x±s)
-
与正常对照组相比,高浓度葡萄糖糖可以明显诱导CFs合成TGF-β1(P < 0.01)。与模型对照组相比,100、50 mg/L丹酚酸A及西药对照组能明显抑制TGF-β1的合成(P < 0.01)(见表 5)。
分组 TGF-β1/(pg/mL) 正常对照组 70.75±5.73 模型对照组 127.46±27.00## 100 mg/L丹酚酸A组 54.18±1.35** 50 mg/L丹酚酸A组 73.70±26.88** 25 mg/L丹酚酸A组 138.87±17.55##▲▲■■ 西药对照组 63.02±11.12**△△ F 20.07 P < 0.01 MS组内 319.632 q检验:与正常对照组比较##P < 0.01;与模型对照组比较**P < 0.01;与100 mg/L丹酚酸A组比较▲▲P < 0.01;与50 mg/L丹酚酸A组比较■■P < 0.01;与25 mg/L丹酚酸A组比较△△P < 0.01 表 5 丹酚酸A对CFs在高浓度葡萄糖培养下TGF-β1合成的影响(ni=6;x±s)
-
与正常对照组相比,高浓度葡萄糖可以诱导CFs中β-catenin蛋白表达明显升高(P < 0.01),且明显下调p-GSK-3β的表达(P < 0.01)。与模型对照组比较,用药组均可明显抑制β-catenin的表达(P < 0.01),100 mg/L丹酚酸A可以上调p-GSK-3β的表达(P < 0.05)(见表 6)。
分组 β-catenin GSK-3β p-GSK-3β 正常对照组 0.203±0.037 0.311±0.015 0.255±0.023 模型对照组 0.493±0.039## 0.336±0.023 0.144±0.282## 100 mg/L丹酚酸A组 0.231±0.024** 0.313±0.028 0.222±0.088* 50 mg/L丹酚酸A组 0.259±0.038#** 0.330±0.016 0.191±0.046# 西药对照组 0.249±0.041#** 0.320±0.023 0.195±0.043# F 62.42 1.50 0.55 P < 0.01 >0.05 >0.05 MS组内 0.001 0.001 0.018 q检验:与正常对照组比较#P < 0.05,##P < 0.01;与模型对照组比较*P < 0.05,**P < 0.01;与100 mg/L丹酚酸A组比较▲P < 0.05;与50 mg/L丹酚酸A组比较■P < 0.05;与25mg/L丹酚酸A组比较△ P < 0.05 表 6 丹酚酸A对CFs在高浓度葡萄糖培养下Wnt信号通路蛋白表达的影响(ni=6;x±s)
-
中药丹参为多年生草本植物丹参的根,据《神农本草经》《本草汇言》《山东中草药手册》等有关丹参的古籍载录,丹参味苦、性微寒,可祛瘀而生新, 虽行但不破, 可补可散, 起活血、止痛、化瘀、养血、生血等作用, 且疗效甚显[8-11]。临床上中医广泛用于治疗心脑血管系统疾病。现代研究[12]发现丹参具有保护脑、器官、中枢神经系统及调节免疫力、抗菌抗炎和抗肿瘤的作用,活性成分丹参酮及丹酚酸类是丹参药理作用的物质基础。
心肌纤维化是形成纤维化的关键效应器,CFs具有分泌功能,在心脏正常生长时和病理性重塑中肩负重要作用[12]。心肌纤维化的病理基础为心肌间质含量所占心肌组织比例增加[13],是DCM病理组织学变化表现之一,主要表现为成纤维细胞数量的增加,心肌组织中胶原过度的沉积进而引发的心室顺应性降低,当舒张功能和收缩功能和受损后,最终会恶化为心力衰竭[14]。
Wnt信号通路异常调控发生时,可限制心肌细胞分化,导致心脏体积变小,阻碍形成分化成心脏的中胚层,影响胚胎心脏发育,诱发纤维增生等疾病[15-17]。β-catenin是Wnt/β-catenin连环蛋白信号转导途径的核心分子,且Wnt信号通路在机体正常条件下处于静默状态,GSK-3β复合物磷酸化的β-catenin会因为泛素蛋白酶识别并降解作用维持在较低水平表达状态。但当信号通路活化后,GSK-3β则会脱离降解复合体,使复合物的形成被抑制,细胞质中β-catenin积累而后进入细胞核并激活靶基因的转录[18]。本实验CFs中Wnt信号通路经高浓度葡萄糖诱导异常激活,β-catenin蛋白表达明显升高,p-GSK-3β的表达明显下调。
TGF-β1为促进心肌纤维化形成和发展的主要细胞因子,并可通过自分泌和旁分泌途径促进成纤维细胞增殖,增加以胶原为主的间质蛋白的合成,也可以促进损伤修复和抑制细胞外基质成分的降解,在形成组织器官纤维化的过程中发挥了作用[19-20]。TGF-β1信号转到通路同时也是各种因素致心肌纤维化的共同通路。本实验中经高浓度葡萄糖糖诱导的CFs促进心肌成纤维细胞的增殖,TGF-β1合成增加。
本研究结果发现,高浓度葡萄糖培养的CFs用丹酚酸A干预后抑制细胞增殖效果明显,S期细胞数量百分比降低明显,表明其干预下能显著抑制CFs增殖,减少CFs数量,并且延缓糖尿病心肌纤维化的发展。进一步实验发现,Ⅰ型胶原、Ⅲ型胶原的分泌还能被其降低,推断丹酚酸A可以抑制CFs增殖的同时,还能够降低胶的原合成与分泌能力,继而推迟了糖尿病心肌纤维化的发展。在分子水平上的实验结果发现,高浓度葡萄糖可以诱导β-catenin和TGF-β1的高表达并下调p-GSK-3β的表达,且丹酚酸A能抑制β-catenin表达、上调p-GSK-3β的表达,表明丹酚酸A能够阻断WNT/β-catenin信号转到通路的异常激活;TGF-β1蛋白的表达水平同时被丹酚酸A抑制,表明丹酚酸A与TGF-β信号通路的转导也存在相应的作用关系。在高糖环境中Wnt信号通路与TGF-β信号通路关键分子的变化指向两种途径之间可能存在协同作用。
综上,丹酚酸A抑制CFs在高浓度葡萄糖中的细胞数量和细胞周期S期的增殖,降低Ⅰ型胶原、Ⅲ型胶原和TGF-β1的分泌,同时能够干预Wnt信号通路的异常表达。提示丹酚酸A是治疗糖尿病心肌纤维化的潜在有效成分,其深入的作用机制值得研究,本研究为中医药防治糖尿病MF研究提供了重要的实验基础。
丹酚酸A对心肌成纤维细胞在高浓度葡萄糖刺激下Wnt信号通路的影响
Effects of salvianolic acid A on Wnt signaling pathway in cardiac fibroblasts stimulated by high concentration glucose
-
摘要:
目的探讨丹酚酸A对高浓度葡萄糖诱导的心肌成纤维细胞(CFs)Wnt信号通路的影响及作用机制。 方法采用高浓度葡萄糖刺激CFs构建细胞增殖模型,以22 mg/L卡托普利为西药对照,不同浓度丹酚酸A处理CFs。MTT比色法检测细胞的增殖能力,流式细胞术分析细胞增殖周期,ELISA法测定细胞中Ⅰ型、Ⅲ型胶原的生成和转化生长因子-β1(TGF-β1)蛋白的分泌,蛋白质印迹法检测β-catenin、GSK-3β、p-GSK-3β蛋白的表达水平。 结果干预24、48 h,与模型对照组相比,25、50、100 mg/L丹酚酸A均可明显抑制细胞增殖(P < 0.01)。与模型对照组相比,25、50、100 mg/L丹酚酸A均能抑制CFs Ⅰ型胶原和Ⅲ型胶原的分泌(P < 0.05~P < 0.01);50、100 mg/L丹酚酸A均能明显抑制TGF-β1的合成及β-catenin的表达(P < 0.01);100 mg/L丹酚酸A可以上调p-GSK-3β的表达(P < 0.05)。 结论丹酚酸A可抑制高浓度葡萄糖诱导的CFs增殖、胶原蛋白分泌和TGF-β1的合成,其机制可能与抑制Wnt信号通路有关。 Abstract:ObjectiveTo investigate the effect and mechanism of salvianolic acid A on Wnt signaling pathway in cardiac fibroblasts(CFs) induced by high concentration glucose. MethodsCell proliferation model was established by stimulating CFs with high concentration glucose, 22 mg/L captopril was used as western medicine control, and CFs were treated with different concentrations of salvianolic acid A.MTT assay was used to detect the proliferation ability of cells, flow cytometry was applied to analyze the cell proliferation cycle, and ELISA was employed to determine the production of type Ⅰ collagen, type Ⅲ collagen and protein secretion of transforming growth factor-β1(TGF-β1), and Western blotting was performed to detect the protein expression level of β-catenin, GSK-3β and p-GSK-3β. ResultsAfter treatment for 24 and 48 hours, compared with the model control group, 25, 50 and 100 mg/L salvianolic acid A could significantly inhibit cell proliferation(P < 0.01).Compared with the model control group, 25, 50 and 100 mg/L salvianolic acid A inhibited the secretion of type Ⅰ collagen and type Ⅲ collagen in CFs(P < 0.05 to P < 0.01);50 and 100 mg/L salvianolic acid A significantly inhibited the TGF-β1 production and β-catenin expression(P < 0.01);100 mg/L salvianolic acid A upregulated p-GSK-3β expression(P < 0.05). ConclusionsSalvianolic acid A can inhibit the proliferation, collagen secretion and TGF-β1 production of CFs induced by high concentration glucose, the mechanism of which may be related to the inhibition of Wnt signaling pathway. -
表 1 高浓度葡萄糖在不同时间点对CFs增殖活性的作用(ni=6;x±s)
分组 OD 24 h 48 h 正常对照组 0.118±0.006 0.142±0.018 模型对照组 0.138±0.010 0.166±0.015 t 4.20 2.51 P < 0.01 < 0.05 表 2 丹酚酸A对CFs在高浓度葡萄糖培养下细胞增殖的影响(ni=6;x±s)
分组 OD 24 h 48 h 正常对照组 0.118±0.006 0.142±0.018 模型对照组 0.138±0.010## 0.166±0.015## 高渗对照组 0.129±0.013 0.150±0.016 100 mg/L丹酚酸A组 0.102±0.002##** 0.114±0.012** 50 mg/L丹酚酸A组 0.118±0.006**▲▲ 0.119±0.008##** 25 mg/L丹酚酸A组 0.126±0.009#**▲▲ 0.131±0.008##**▲ 西药对照组 0.080±0.003##**▲▲■■△△ 0.068±0.002##**▲▲■ ■△△ F 36.25 38.88 P < 0.01 < 0.01 MS组内 0.000 0.000 q检验:与正常对照组比较#P < 0.05,##P < 0.01;与模型对照组比较**P < 0.01;与100 mg/L丹酚酸A组比较▲P < 0.05,▲▲P < 0.01;与50 mg/L丹酚酸A组比较■■P < 0.01;与25 mg/L丹酚酸A组比较△△P < 0.01 表 3 丹酚酸A对CFs在高浓度葡萄糖培养下细胞增殖周期的影响(ni=6;x±s)
分组 细胞周期(G0+G1)/% 细胞周期(S+G2+M)/% 正常对照组 97.131±0.530 2.869±0.530 模型对照组 88.987±0.929## 11.013±0.929## 100 mg/L丹酚酸A组 96.628±0.035** 3.372±0.035** 50 mg/L丹酚酸A组 92.533±0.728##**▲▲ 7.467±0.728##**▲▲ F 104.74 104.71 P < 0.01 < 0.01 MS组内 0.419 0.419 q检验:与正常对照组比较##P < 0.01;与模型对照组比较**P < 0.01;与100 mg/L丹酚酸A组比较▲▲P < 0.01 表 4 丹酚酸A对CFs在高浓度葡萄糖培养下Ⅰ型胶原、Ⅲ型胶原分泌的影响(ni=6;x±s)
分组 Ⅰ型胶原/(pg/mL) Ⅲ型胶原/(ng/mL) 正常对照组 628.11±126.89 5.31±0.24 模型对照组 2 081.69±525.70## 10.00±0.96## 100 mg/L丹酚酸A组 1 359.87±59.15##** 6.18±1.48##** 50 mg/L丹酚酸A组 1 361.94±145.35##** 6.87±2.61** 25 mg/L丹酚酸A组 1 624.49±38.06##* 6.95±1.44** 西药对照组 1 834.19±168.65##▲■ 10.12±1.12##▲▲■ ■△△ F 17.46 9.37 P < 0.01 < 0.01 MS组内 57 829.716 2.217 q检验:与正常对照组比较##P < 0.01;与模型对照组比较*P < 0.05,**P < 0.01;与100 mg/L丹酚酸A组比较▲P < 0.05,▲▲P < 0.01;与50 mg/L丹酚酸A组比较■P < 0.05,■■P < 0.01;与25 mg/L丹酚酸A组比较△△P < 0.01 表 5 丹酚酸A对CFs在高浓度葡萄糖培养下TGF-β1合成的影响(ni=6;x±s)
分组 TGF-β1/(pg/mL) 正常对照组 70.75±5.73 模型对照组 127.46±27.00## 100 mg/L丹酚酸A组 54.18±1.35** 50 mg/L丹酚酸A组 73.70±26.88** 25 mg/L丹酚酸A组 138.87±17.55##▲▲■■ 西药对照组 63.02±11.12**△△ F 20.07 P < 0.01 MS组内 319.632 q检验:与正常对照组比较##P < 0.01;与模型对照组比较**P < 0.01;与100 mg/L丹酚酸A组比较▲▲P < 0.01;与50 mg/L丹酚酸A组比较■■P < 0.01;与25 mg/L丹酚酸A组比较△△P < 0.01 表 6 丹酚酸A对CFs在高浓度葡萄糖培养下Wnt信号通路蛋白表达的影响(ni=6;x±s)
分组 β-catenin GSK-3β p-GSK-3β 正常对照组 0.203±0.037 0.311±0.015 0.255±0.023 模型对照组 0.493±0.039## 0.336±0.023 0.144±0.282## 100 mg/L丹酚酸A组 0.231±0.024** 0.313±0.028 0.222±0.088* 50 mg/L丹酚酸A组 0.259±0.038#** 0.330±0.016 0.191±0.046# 西药对照组 0.249±0.041#** 0.320±0.023 0.195±0.043# F 62.42 1.50 0.55 P < 0.01 >0.05 >0.05 MS组内 0.001 0.001 0.018 q检验:与正常对照组比较#P < 0.05,##P < 0.01;与模型对照组比较*P < 0.05,**P < 0.01;与100 mg/L丹酚酸A组比较▲P < 0.05;与50 mg/L丹酚酸A组比较■P < 0.05;与25mg/L丹酚酸A组比较△ P < 0.05 -
[1] GALDERISI M. Diastolic dysfunction and diabetic cardiomyopathy: evaluation by Dopple echocardiography[J]. J Am Coll Cardiol, 2006, 48(8): 1548. [2] 黄巧丽, 周华, 李涛. Wnt信号通路与心脏发育和心肌诱导分化[J]. 浙江师范大学学报(自然科学版), 2016, 39(3): 331. [3] EHRLUND A, MEJHERT N, LORENTE-CEBRIÁN S, et al. Characterization of the wnt inhibitors secreted frizzled-related proteins(SFRPs) in human adipose tissue[J]. J Clin Endocrinol Metab, 2013, 98(3): E503. doi: 10.1210/jc.2012-3416 [4] TAO H, YANG JJ, SHI KH, et al. Wnt signaling pathway in cardiac fibrosis: new insights and directions[J]. Metabolism, 2016, 65(2): 30. doi: 10.1016/j.metabol.2015.10.013 [5] 高波. 丹参的药理分析及临床应用研究[J]. 中国卫生标准管理, 2016, 7(9): 119. [6] 陈梅. 丹参分散片的质量研究[J]. 蚌埠医学院学报, 2015, 40(8): 1096. [7] SREEJIT P, KUMAR S, VERMA RS. An improved protocol for primary culture of cardiomyocyte from neonatal mice[J]. In Vitro Cell Dev Biol, 2008, 44(3/4): 45. [8] LEASK A, PARAPURAM SK, SHI WX, et al. Connective tissue growth factor(CTGF, CCN2) gene regulation: a potent clinical biomarker of fibroprolifer active disease[J]. J Cell Commun Signal, 2009, 3(2): 89. doi: 10.1007/s12079-009-0037-7 [9] 高兵. 丹参的药理作用及临床应用分析[J]. 中国现代药物应用, 2018, 12(1): 196. [10] 孙宁远, 朱雪林, 陈君. 丹参化学成分抗纤维化药理作用及机制研究进展[J]. 中国实验方剂学杂志, 2020, 26(22): 201. [11] 王涵, 杨娜, 谭静, 等. 丹参化学成分、药理作用及临床应用的研究进展[J]. 特产研究, 2018, 40(1): 48. [12] 蒲翔, 姚元贵, 谢宇, 等. 丹参破壁饮片、传统饮片中水溶性成分对心肌细胞保护作用对比研究[J]. 时珍国医国药, 2020, 31(6): 1354. doi: 10.3969/j.issn.1008-0805.2020.06.021 [13] 张飞飞, 党懿, 郝清卿, 等. 心脏收缩力调节对转化生长因子β1/结缔组织生长因子信号通路的影响[J]. 中华老年心脑血管病杂志, 2018, 20(5): 525. doi: 10.3969/j.issn.1009-0126.2018.05.019 [14] 高嘉梦, 胡兵, 申锷. 心肌成纤维细胞转分化与糖尿病心肌病的研究进展[J]. 中华心血管病杂志, 2020, 48(10): 885. doi: 10.3760/cma.j.cn112148-20191027-00659 [15] GOLDSMITH EC, BRADSHAW AD, SPINALE FG. Cellular mechanisms of tissue fibrosis. 2. contributory pathways leading to myocardial fibrosis: moving beyond collagen expression[J]. Am J Physiol, 2013, 304(5): C393. doi: 10.1152/ajpcell.00347.2012 [16] MAC DONALD BT, TAMAI K, HE X. Wnt/β-catenin signaling: components, mechanisms, and diseases[J]. Dev Cell, 2009, 17(1): 9. [17] PENKE LR, PETERS GM. Molecular determinants of mesenchymal cell activation in fibroproliferative diseases[J]. Cell Mol Life Sci, 2019, 76(21): 4179. doi: 10.1007/s00018-019-03212-3 [18] SHARMA AK, THANIKACHALAM PV, BHATIA S. The signaling interplay of GSK-3β in myocardial disorders[J]. Drug discov today, 2020, 25(4): 633. doi: 10.1016/j.drudis.2020.01.017 [19] 张建奇, 张明, 吴熙, 等. Elabela-APJ轴在心血管系统疾病中的作用[J]. 国际心血管病杂志, 2020, 47(5): 281. doi: 10.3969/j.issn.1673-6583.2020.05.007 [20] VALLÉE A, LECARPENTIER Y. TGF-β in fibrosis by acting as a conductor for contractile properties of myofibroblasts[J]. Cell Bioscl, 2019, 9(1): 98. doi: 10.1186/s13578-019-0362-3 -





 下载:
下载: