-
原发性高血压是缺血性心肌病最重要的危险因素之一,现有研究[1]表明,高血压合并的心肌梗死是由遗传因素和环境因素等综合作用的结果。肾素-血管紧张素系统(RAS)不仅在高血压发病机制中发挥了重要作用,而且是高血压诱发心肌梗死过程中重要的影响因子。人血管紧张素Ⅱ受体1(AGTR1)介导了血管紧张素AngⅡ主要效应的发生[2],所以在高血压的研究中AGTR1基因一直是研究的重点。本研究对AGTR1 A1166C基因多态性在健康成人、高血压病人、高血压合并心肌梗死病人间的分布频率进行比较,以探讨AGTR1基因和高血压合并心肌梗死的相关性。现作报道。
-
选取2017-2018年我院体检中心体检的健康成人121名作为正常组;选择同期体检中心体检的高血压病人105例作为高血压组;选择同期急诊收治的高血压合并心肌梗死病人95例作为高血压合并心肌梗死组(合并组)。合并组纳入标准:(1)原发性高血压合并心肌梗死病人,其中原发性高血压诊断标准为收缩压≥140 mmHg和/或舒张压≥90 mmHg,且经心电图和心肌酶检测确诊为急性心肌梗死;(2)病人无高血压肾病等高血压并发症;(3)病人无脑梗死或者心肌梗死等血栓病史;(4)病人无精神障碍疾病;(5)自愿入组。排除标准:(1)继发性高血压;(2)既往有缺血性卒中、心肌梗死病史或血栓栓塞性疾病;(3)患有高血压肾病等高血压继发性疾病;(4)妊娠期、哺乳期妇女;(5)精神障碍疾病。本研究经医院伦理委员会论证同意,病人均知情同意,并签署知情同意书。
-
病人禁食12 h后取外周静脉血5 mL,采用DNA提取试剂盒提取外周血总DNA,引物设计按照Doria等设计,引物1:5′-CAC CAT GTT TTG AGG TT-3′;引物2:5′-CGA GTT TCT GAC ATT GTT C-3′。PCR扩增目的片段基因,反应步骤:95 ℃预变性10 min,95 ℃变性30 s,58 ℃退火30 s,72 ℃延伸30 s,共循环30次,72 ℃终末循环10 min,最后在4 ℃终止反应。A1166C的变异导致Dde Ⅰ限制性内切酶切位点的出现,PCR产物用Dde Ⅰ在37 ℃酶切1 h。2%琼脂糖凝胶电泳(恒压120 V,电泳液为1×TAE),紫外灯下观察结果。
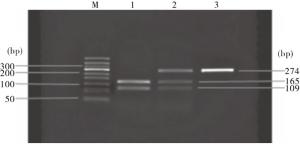
PCR扩增产物为AGTR1 3′端非编码区5′末端1 058~1 331 bp之间274 bp的DNA。扩增产物中无A1166C突变切点则为274 bp,若扩增片段中存在A-C碱基替换则产生Dde Ⅰ切点,经过酶切后产生165 bp和109 bp的片段。AA基因有一条274 bp片段,CC基因含有165 bp和109 bp 2条片段,含有以上三条片段的为AC杂合基因。电泳结果见图 1。
-
采用方差分析、q检验、χ2检验、秩和检验和Fisher′s确切概率法。
-
3组性别、年龄、体质量差异均无统计学意义(P>0.05),高血压组和合并组舒张压、收缩压均高于正常组(P < 0.05),高血压组与合并组舒张压、收缩压和糖尿病、高血脂患病情况差异均无统计学意义(P>0.05)(见表 1)。
分组 n 男 女 年龄/岁 体质量/kg 收缩压/mmHg 舒张压/mmHg 糖尿病 高血脂 正常组 121 63 58 62.7±9.4 68.5±5.3 116.2±8.3 73.1±4.04 — — 高血压组 105 48 57 64.8±8.3 70.2±6.7 151.6±18.4* 87.2±7.84* 42(40.0) 55(52.4) 合并组 95 49 46 63.6±9.0 69.7±7.0 151.1±17.9* 89.2±7.20* 40(42.1) 52(54.7) χ2 — 1.07 1.56△ 2.18△ 201.41△ 207.71△ 0.09 0.11 P — >0.05 >0.05 >0.05 < 0.01 < 0.01 >0.05 >0.05 △示F值;q检验:与正常组比较*P < 0.05 表 1 3组病人一般资料比较[n;百分率(%)]
-
正常组、高血压组和合并组的基因型分布符合Hardy-Weinberg平衡(P>0.05);3组基因型分布差异有统计学意义(P < 0.01),A等位基因与C等位基因差异无统计学意义(P>0.05)(见表 2)。
分组 n 基因型 等位基因 AA AC CC A C 正常组 121 102(84.30) 19(15.70) 0(0.00) 223(92.15) 19(7.85) 高血压组 105 93(88.57) 12(11.43) 0(0.00) 198(94.29) 12(5.71) 合并组 95 82(86.32) 8(8.42) 5(5.26) 172(90.53) 18(9.47) χ2 — 14.40 2.03 P — < 0.01 >0.05 表 2 3组基因型和等位基因分布[n;百分率(%)]
-
按照高血压分级标准:1级高血压(轻度),收缩压140~159 mmHg或舒张压90~99 mmHg;2级高血压(中度),收缩压160~179 mmHg或舒张压100~109 mmHg;3级高血压(重度),收缩压≥180 mmHg或舒张压≥110 mmHg;单纯收缩期高血压,收缩压≥140 mmHg和舒张压 < 90 mmHg。合并组不同高血压分级病人AA基因和等位基因A分布频率间差异均有统计学意义(P < 0.05)(见表 3)。
分组 n 高血压分级 基因型频率 等位基因频率 AA AC CC A C 高血压组 105 1级 62(59.05) 0(0.00) 0(0.00) 124(59.05) 0(0.00) 2级 31(29.52) 4(3.81) 0(0.00) 66(31.43) 4(1.90) 3级 0(0.00) 8(7.62) 0(0.00) 8(3.81) 8(3.81) 单纯性 0(0.00) 0(0.00) 0(0.00) 0(0.00) 0(0.00) 合并组 95 1级 42(44.21) 0(0.00) 0(0.00) 84(44.21) 0(0.00) 2级 40(42.11) 3(3.16) 0(0.00) 83(43.68) 3(1.58) 3级 0(0.00) 5(5.26) 5(5.26) 5(2.63) 15(7.89) 单纯性 0(0.00) 0(0.00) 0(0.00) 0(0.00) 0(0.00) uc — 2.07 — — 2.44 — P — < 0.05 >0.05△ — < 0.05 >0.05△ △示Fisher′s确切概率法 表 3 合并组不同高血压分级病人AGTR1 A1166C多态性[n;百分率(%)]
-
肾素-血管紧张素-醛固酮系统相关的基因一直是被认为原发性高血压,肾性高血压病发病的重要调控基因[3-5],因为该系统对于全身和肾脏内的血流动力学有着显著的调控作用,而高血压一直被认为是心肌梗死发生的独立高危因素之一。在高血压病人中AngⅡ可以通过激活血管紧张素受体和下游通路[6-7],引起血压的增高。在改善高血压的状态后,应用RAAS抑制剂可以明显改善心肌梗死的发生,但是仍然有相当一部分病人在血压控制良好的情况下仍然出现心肌梗死,这表明高血压合并心肌梗死的发生可能存在个体易感性。
人类AGTR1基因位于3q21~25,仅含有一个外显子结构,A1166C位于3端的非编码区,不编码蛋白,但是可能对于基因的调控转录和翻译发挥作用。目前对于AGTR A1166C基因多态性对于高血压和心肌梗死的发生关系鲜有报道,从生物学上看,AngⅡ的作用主要由AGTR1介导[7-9],AGTR1主要分布在成人血管、肾、心、脑、肝等部位,和血流动力的调节密切相关[10-11]。
本研究以临床中病人为研究对象,从病人资料来看,体检中心体检健康成人和高血压病人以及高血压合并心肌梗死的病人,在性别、年龄等方面无明显差别,排除了年龄等因素造成的结果不准确。基因多态性结果显示,3组基因型分布差异有统计学意义,A等位基因与C等位基因差异无统计学意义。提示AGTR1基因可能高血压合并心肌梗死发生的易感基因。在高血压分级合并心肌梗死中发现,合并组不同高血压分级病人AA基因和等位基因A分布频率间差异均有统计学意义(P < 0.05)。其中A等位基因在1、2级高血压病人中频率较高,而C主要在3级高血压中频率较高,提示高血压分级也可能与该等位基因分布频率有关,相关等位基因频率变高可能会导致心肌梗死的发生。
综上,本文通过探讨AGTR1与高血压合并心肌梗死的关系,发现AGTR A1166C基因多态性与心肌梗死的发生有一定关系,对于高血压病人进行心肌梗死易感性筛查有一定意义,对临床诊断和预防心肌梗死有借鉴价值,但是由于基因作用的复杂性,AGTR1基因与心肌梗死发生关系还有待进一步研究。
血管紧张素Ⅱ受体1基因多态性与高血压合并心肌梗死发生的相关性
Correlation between the genetic polymorphism of angiotensin Ⅱ receptor 1 and occurrence of hypertension complicated with myocardial infarction
-
摘要:
目的探讨人血管紧张素Ⅱ受体1(AGTR1)A1166C多态性和高血压合并心肌梗死的关系。 方法采用聚合酶链反应-限制性片段长度多态性技术,检测并比较AGTR1多态性在健康体检成人(正常组,121名)、高血压病人(高血压组,105例)、高血压合并心肌梗死病人(合并组,95例)中的分布情况。 结果正常组、高血压组和合并组的基因型分布符合Hardy-Weinberg平衡(P>0.05);3组基因型间分布差异有统计学意义(P < 0.01),A等位基因与C等位基因差异无统计学意义(P>0.05)。合并组不同高血压分级病人AA基因和等位基因A分布频率间差异均有统计学意义(P < 0.05)。 结论AGTR1 A1166C基因多态性与高血压合并心肌梗死有关,C等位基因携带可能增加高血压合并心肌梗死的发生风险。 -
关键词:
- 高血压 /
- 心肌梗死 /
- 人血管紧张素Ⅱ受体1 /
- 基因多态性
Abstract:ObjectiveTo investigate the relationship between the polymorphism of human angiotensin Ⅱ receptor 1(AGTR1) A1166C and hypertension complicated with myocardial infarction. MethodsThe distribution of AGTR1 polymorphisms in healthy adults(normal group, 121 subjects), hypertension patients(hypertension group, 105 cases) and hypertension complicated with myocardial infarction(combined group, 95 cases) were detected and compared using polymerase chain reaction restriction fragment length polymorphism technique. ResultsThe distribution of genotypes in the normal group, hypertension group and combined group were accorded with the Hardy-Weinberg equilibrium(P>0.05).The differences of the distribution of genotypes among three groups were statistically significant(P < 0.01), but there was no statistical significance between A allele and C allele among three groups(P>0.05).The differences of the AA gene and A allele gene distribution frequency were statistically significant in the combined group with different hypertension grades(P < 0.05). ConclusionsThe AGTR1 A1166C gene polymorphism is associated with hypertension complicated with myocardial infarction, and the C allele carrying may increase the risk of hypertension complicated with myocardial infarction. -
表 1 3组病人一般资料比较[n;百分率(%)]
分组 n 男 女 年龄/岁 体质量/kg 收缩压/mmHg 舒张压/mmHg 糖尿病 高血脂 正常组 121 63 58 62.7±9.4 68.5±5.3 116.2±8.3 73.1±4.04 — — 高血压组 105 48 57 64.8±8.3 70.2±6.7 151.6±18.4* 87.2±7.84* 42(40.0) 55(52.4) 合并组 95 49 46 63.6±9.0 69.7±7.0 151.1±17.9* 89.2±7.20* 40(42.1) 52(54.7) χ2 — 1.07 1.56△ 2.18△ 201.41△ 207.71△ 0.09 0.11 P — >0.05 >0.05 >0.05 < 0.01 < 0.01 >0.05 >0.05 △示F值;q检验:与正常组比较*P < 0.05 表 2 3组基因型和等位基因分布[n;百分率(%)]
分组 n 基因型 等位基因 AA AC CC A C 正常组 121 102(84.30) 19(15.70) 0(0.00) 223(92.15) 19(7.85) 高血压组 105 93(88.57) 12(11.43) 0(0.00) 198(94.29) 12(5.71) 合并组 95 82(86.32) 8(8.42) 5(5.26) 172(90.53) 18(9.47) χ2 — 14.40 2.03 P — < 0.01 >0.05 表 3 合并组不同高血压分级病人AGTR1 A1166C多态性[n;百分率(%)]
分组 n 高血压分级 基因型频率 等位基因频率 AA AC CC A C 高血压组 105 1级 62(59.05) 0(0.00) 0(0.00) 124(59.05) 0(0.00) 2级 31(29.52) 4(3.81) 0(0.00) 66(31.43) 4(1.90) 3级 0(0.00) 8(7.62) 0(0.00) 8(3.81) 8(3.81) 单纯性 0(0.00) 0(0.00) 0(0.00) 0(0.00) 0(0.00) 合并组 95 1级 42(44.21) 0(0.00) 0(0.00) 84(44.21) 0(0.00) 2级 40(42.11) 3(3.16) 0(0.00) 83(43.68) 3(1.58) 3级 0(0.00) 5(5.26) 5(5.26) 5(2.63) 15(7.89) 单纯性 0(0.00) 0(0.00) 0(0.00) 0(0.00) 0(0.00) uc — 2.07 — — 2.44 — P — < 0.05 >0.05△ — < 0.05 >0.05△ △示Fisher′s确切概率法 -
[1] SALVADOR GL, MARMENTINI VM, COSMO WR, et al. Angiotensin-converting enzyme inhibitors reduce mortality compared to angiotensin receptor blockers: systematic review and meta-analysis[J]. Eur J Prev Cardiol, 2017, 24(18): 1914. doi: 10.1177/2047487317728766 [2] BAO X, ZHU W, ZHANG R, et al. Synthesis and evaluation of novel angiotensin Ⅱ receptor 1 antagonists as anti-hypertension drugs[J]. Bioorg Med Chem, 2016, 24(9): 2023. doi: 10.1016/j.bmc.2016.03.028 [3] WATANABE R, SUZUKI JI, WAKAYAMA K, et al. Angiotensin Ⅱ receptor blocker irbesartan attenuates cardiac dysfunction induced by myocardial infarction in the presence of renal failure[J]. Hypertens Res, 2016, 39(4): 237. doi: 10.1038/hr.2015.141 [4] 张源波, 李海明, 杨萌, 等. 利尿钠肽及肾素-血管紧张素-醛固酮系统对高血压的影响[J]. 中国循证心血管医学杂志, 2017, 9(11): 129. [5] 岳薇薇, 胡大春. 肾素-血管紧张素-醛固酮系统在高血压遗传病理机制中的研究进展[J]. 医学综述, 2018, 24(22): 4440. doi: 10.3969/j.issn.1006-2084.2018.22.014 [6] 赵耀武, 艾力江·热西提, 李熙. 继发性高血压患者尿微量蛋白含量与肾素-血管紧张素-醛固酮系统中肾素的关系研究[J]. 中华养生保健, 2020, 38(2): 94. [7] HASS A, OZ H, MASHAVI M, et al. Role of RAAS and adipokines in cardiovascular protection: effect of different doses of angiotensin Ⅱ receptor blocker on adipokines level in hypertensive patients[J]. J Am Soc Hypertens, 2014, 8(10): 709. doi: 10.1016/j.jash.2014.07.033 [8] AMEER OZ, BUTLIN M, KASCHINA E, et al. Long-term angiotensin Ⅱ receptor blockade limits hypertension, aortic dysfunction, and structural remodeling in a rat model of chronic kidney disease[J]. J Vasc Res, 2016, 53(3/4): 216. [9] LIN J, LIN S, WU Y, et al. Hypomethylation of the angiotensin Ⅱ type Ⅰ receptor (AGTR1) gene along with environmental factors increases the risk for essential hypertension[J]. Cardiology, 2017, 137(2): 126. doi: 10.1159/000458520 [10] SINGH A, SRIVASTAVA N, YADAV A, et al. Targeting AGTR1/NF-κB/CXCR4 axis by miR-155 attenuates oncogenesis in glioblastoma[J]. Neoplasia, 2020, 22(10): 497. doi: 10.1016/j.neo.2020.08.002 [11] YANG Y, ZHOU Y, CAO Z, et al. miR-155 functions downstream of angiotensin Ⅱ receptor subtype 1 and calcineurin to regulate cardiac hypertrophy[J]. Exp Ther Med, 2016, 12(3): 1556. doi: 10.3892/etm.2016.3506 -




 下载:
下载:


