-
类风湿性关节炎(rheumatoid arthritis, RA)是常见的自身免疫性疾病,骨破坏贯穿整个病程,是病人致残的主要原因。RA骨破坏呈慢性进展性,以滑膜炎为主要病理变化,关节滑膜产生慢性持续性的炎症和增生,形成血管翳,继而侵犯关节软骨、软骨下骨、韧带和肌腱等,造成不可逆的骨破坏[1-2]。不仅严重影响病人生活质量,也为病人及其家属带来了极大的痛苦和经济负担,最终导致严重的社会问题。现代医学研究[3-5]发现,腺苷酸活化蛋白激酶(AMP-activated protein kinase, AMPK)、核因子κB受体活化因子配体(RANKL)信号通路及白细胞介素-6(IL-6)、肿瘤坏死因子α(TNF-α)等促炎细胞因子与RA骨破坏关系密切,相互介导着RA骨破坏的发生发展。目前,RA骨破坏仍大多数基于传统的治疗方案,包括非甾体类抗炎药(NSAIDS)、抗风湿药物(DMARDs)、糖皮质激素类药物(GCS)及最新的生物治疗。但由于NSAIDS、DMARDs、GCS等药物长期服用有严重的不良反应,生物制剂价格高昂且疗效需进一步证实,尤其是应用于活动性低的RA病人的临床试验中收效甚微[1, 6],这些都限制了RA骨破坏的治疗。因此,寻找新的治疗RA骨破坏的药物仍然是临床面临的挑战性问题。
近年来的研究[7-8]表明,二甲双胍能够抑制全身性炎症,影响各种炎症因子水平,通过多种途径影响骨代谢,起到骨质保护作用,但具体机制尚不明确。并且针对二甲双胍对RA导致的骨破坏的作用效果及相关机制研究以及二甲双胍是否可以用于治疗RA导致骨破坏等内容,学术界尚无定论。本研究通过建造动物模型,测定佐剂性关节炎(adjuvant arthritis, AA)大鼠的整体指标、血清骨代谢指标、放射线检查、关节病理免疫组织化学(免疫组化)等指标,探究二甲双胍治疗RA导致的骨破坏的效果及机制,为临床治疗提供新的思路。
-
将10 mg/mL完全弗氏佐剂(complete freund adjuvant, CFA)充分混匀,于每只大鼠右后足跖皮下注射CFA 0.1 mL制备AA模型。2周后把建模成功的大鼠筛选出40只, 每组8只,随机分为模型组、甲氨蝶呤(methotrexate, MTX)组(0.5 mg·kg-1·3 d-1)、二甲双胍高剂量组(100 mg·kg-1·d-1)、二甲双胍中剂量组(75 mg·kg-1·d-1)、二甲双胍低剂量组(50 mg·kg-1·d-1)。正常组用0.9%氯化钠溶液同法灌胃给药,给药时间均持续30 d。
-
试剂:CFA购自Chondrex Inc(USA);二甲双胍片(格华止)购自中美上海施贵宝制药有限公司;MTX购自通化茂祥制药有限公司。大鼠血钙ELISA检测试剂盒、大鼠血磷ELISA检测试剂盒、大鼠OPG ELISA检测试剂盒、大鼠RANKL ELISA检测试剂盒,购自上海酶联生物科技有限公司,多聚甲醛、苏木精、伊红、切片石蜡、中性树胶、无水乙醇、二甲苯、磷酸氢二钠、氯化钠均购自上海麦克林生化科技有限公司;磷酸盐缓冲液购自北京索莱宝科技有限公司;抗原修复液、免疫组化二抗、DAB显色试剂盒购自北京索莱宝科技有限公司;免疫染色封闭液购自上海碧云天生物技术有限公司。仪器:小动物成像X线机器(布鲁克全自动临床前小动物成像系统,型号in vivo FX PRO, 美国);Olympus AU2700型全自动生化分析仪;大鼠ELISA检测测试仪器(酶标分析仪:Rayto RT-6100);LEICA 2235型轮转切片机(德国LEICA);MICROM HM525型冷冻切片机(德国MICROM);LEICA AUTOSTAINER XL全自动染色机(德国LEICA);MICROM EC350-1冷热台包埋机(德国MICROM);LEICA ASP300S全自动生物组织脱水机(德国LEICA);TEC2500病理组织烘漂仪(常州市郝思琳医用仪器有限公司)。
-
全身评分,从炎症出现后,每隔3~4 d进行全身表现评分,评分标准包括,耳: 0分=无结节和发红症状,1分=一只耳朵结节和发红症状,2分=两只耳朵结节和发红症状; 鼻: 0分=无结缔组织肿胀,1分=明显结缔组织肿胀; 尾: 0分=无结节,1分=有结节; 前足爪: 0分=无肿胀,1分=一个前足爪肿胀,2分=两个前足爪肿胀; 后足爪: 0分=无肿胀,1分=一个后足爪肿胀,2分=两个后足爪肿胀;每只大鼠最多评8分[9]。
-
评价关节周围软组织肿胀的严重程度及关节间隙狭窄、骨质疏松等情况,用10%水合氯醛在CFA免疫后第30天进行麻醉。对继发炎症关节和后足通过X射线成像进行检查。
-
通过ELISA法对大鼠外周血中血钙、血磷、骨保护素(OPG)、RANKL指标进行测定。
-
切片脱蜡至水:经二甲苯Ⅰ、Ⅱ、Ⅲ,3次,每次5 min,要确保二甲苯足量有效;无水乙醇2次,每次5 min;95%乙醇2次,每次5 min;蒸馏水2次,每次5 min。采用枸橼酸抗原修复法热修复后冷却至室温,1×PBS洗3次,每次5 min。免疫染色封闭液室温封闭15 min,封闭后甩掉封闭液,不洗,加一抗孵育,4 ℃过夜。室温平衡30 min,PBS洗3次,每次5 min,二抗孵育,37 ℃,30 min;PBS洗3次,每次5 min,DAB显色,显微镜下观察确定显色终点;显色完毕苏木精复染核2 min,自来水返蓝,梯度浓度乙醇脱水,二甲苯透明,中性树胶封片。并使用Image ProPlus软件对免疫组化结果进行半定量分析,平均光密度值(IOD/area)=累积吸光度值/测量的染色区域的面积,数值越大表示阳性越强,每个实验组2个样品。
-
采用方差分析和q检验。
-
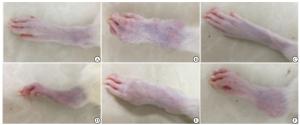
造模30d时,模型组与正常组相比,继发侧踝关节到趾关节出现红斑和重度肿胀,MTX组与模型组相比,肿胀程度明显减轻。二甲双胍各剂量组,相较于模型组,能够明显改善继发侧踝关节肿胀,并且随着二甲双胍剂量的升高,改善程度越明显(见图 1)。
-
从炎症出现后,每隔3 d进行全身评分,在病程17 d左右,AA大鼠全身炎症表现达到高峰,表现为对侧(左后肢)明显。在21 d左右开始,除模型组外,各给药组大鼠出现全身评分降低,模型组在第24天开始出现评分降低。从病程17 d开始,MTX组和二甲双胍各剂量组大鼠全身评分均低于模型组,差异有统计学意义(P < 0.05~P < 0.01)(见表 1)。
分组 n 14 d 17 d 21 d 24 d 27 d 30 d 模型组 8 1.25±0.46 7.50±0.53 7.63±0.52 7.25±0.46 7.13±0.64 5.88±0.64 MTX组 8 1.13±0.35 6.13±0.64** 5.13±0.64** 4.75±0.46** 4.13±0.83** 3.25±0.71** 药物高剂量组 8 1.25±0.46 6.50±0.93** 4.75±0.71** 4.50±0.53** 4.00±0.53** 3.50±0.53** 药物中剂量组 8 1.25±0.49 6.00±0.98** 5.25±0.79** 4.63±0.53** 4.13±0.38** 3.88±0.49** 药物低剂量组 8 1.25±0.46 6.63±0.92* 6.00±0.76** 5.50±0.53** 5.25±0.71** 5.13±0.64** F — 0.12 4.14 21.93 41.32 34.95 27.65 P — >0.05 <0.01 <0.01 <0.01 <0.01 <0.01 MS组内 — 0.200 0.672 0.477 0.253 0.406 0.369 q检验:与模型组比较*P < 0.05, **P < 0.01 表 1 各组大鼠全身评分的变化(x±s;分)
-
药物治疗2周,麻醉后对各组大鼠进行后足X线检查显示,造模成功,大鼠出现了RA骨破坏,二甲双胍可以改善大鼠后足的软组织肿胀及骨缺失,并可改善AA大鼠骨破坏(见图 2)。
-
结果显示,高剂量二甲双胍可以提高AA大鼠血清钙、磷水平,不同剂量二甲双胍均可以提高OPG,降低RANKL的水平,差异均有统计学意义(P < 0.01)(见表 2)。血清骨代谢指标的变化反映了二甲双胍可以改善AA大鼠骨破坏。
分组 n 钙/(mmol/L) 磷/(mmol/L) OPG/ (pg/mL) RANKL/(pg/mL) 正常组 8 2.7±0.07 2.39±0.09 1 853.97±184.12 9.86±0.98 模型组 8 2.46±0.05## 2.05±0.06## 623.39±92.72## 20.65±1.59## MTX组 8 2.63±0.08** 2.21±0.09** 1 357.45±146.49** 10.46±1.23** 药物高剂量组 8 2.61±0.05** 2.18±0.08** 1 333.12±80.65** 10.45±1.83** 药物中剂量组 8 2.56±0.07 2.13±0.1 1 001.88±69.65** 14.28±0.78** 药物低剂量组 8 2.48±0.09 2.1±0.07 840.78±56.41** 16.21±0.79** F — 13.87 16.52 118.0 90.89 P — < 0.01 < 0.01 < 0.01 < 0.01 MS组内 — 0.005 0.007 13 082.354 1.597 q检验:与正常组比较##P < 0.01;与模型组比较**P < 0.01 表 2 各组大鼠血清骨代谢相关指标水平的比较(x±s)
-
每只大鼠选择组织切片1张,采用显微镜显影系统,采集图像。大鼠膝关节AMPK免疫组化结果显示:正常组大鼠的关节组织中,滑膜细胞呈纺锤状,细胞核呈蓝色,AMPK阳性表达部位呈棕黄色。二甲双胍高、中剂量组,AMPK免疫组化染色呈现出棕色,部分区域可见褐色,表达亦呈强阳性,但免疫组化染色与正常组相比较减弱。模型组与正常组及二甲双胍各剂量组比较,AMPK免疫组化染色偶而可见阳性细胞,染色区域显著降低,染色深度也明显减弱(见图 3)。大鼠关节IL-6免疫组化结果显示:正常组大鼠的关节组织中,纺锤状滑膜细胞细胞核大多呈蓝色,IL-6阳性表达部位呈棕黄色。模型组中,IL-6免疫组化染色呈现出棕黄色,表达呈强阳性。二甲双胍各剂量组,IL-6免疫组化染色滑膜细胞偶而可见阳性细胞,大部分与正常组一样呈阴性表达(见图 4)。大鼠关节TNF-α免疫组化结果显示:正常组大鼠的关节组织中,纺锤状梭型滑膜细胞细胞核呈蓝色,TNF-α阳性表达部位呈棕黄色,以阴性表达为主。模型组中,TNF-α免疫组化大量组织染色呈现出棕黄色,表达呈强阳性。二甲双胍各剂量组中,尤其是二甲双胍高剂量组TNF-α免疫组化染色偶而可见阳性细胞,大部分与正常组一样呈阴性表达(见图 5)。对免疫组化结果进行半定量分析结果显示,二甲双胍高、中剂量可提高AA大鼠关节免疫组化AMPK蛋白表达;二甲双胍各剂量均可降低AA大鼠关节免疫组化IL-6蛋白表达;二甲双胍高、中剂量可以降低AA大鼠关节免疫组化TNF-α蛋白表达,差异均有统计学意义(P < 0.01)(见表 3)。
分组 n AMPK IL-6 TNF-a 正常组 8 53.29±9.9 40.44±9.16 95.17±15.07 模型组 8 23.88±5.82## 501.52±86.14## 168.16±23.24## MTX组 8 48.65±4.69** 55.40±9.95** 115.96±10.55** 药物高剂量组 8 47.21±3.36** 54.31±13.46** 116.37±15.12** 药物中剂量组 8 40.71±3.69** 134.07±19.83** 124.37±24.26** 药物低剂量组 8 32.85±7.36 166.96±28.79** 149.27±21.45 F — 25.04 163.9 15.30 P — < 0.01 < 0.01 < 0.01 MS组内 — 38.826 1 501.000 359.300 q检验:与正常组比较##P < 0.01;与模型组比较**P < 0.01 表 3 各组免疫组化结果(AMPK、IL-6、TNF-α)半定量分析(x±s)
-
RA的主要病变特征是全身及受累关节周围骨丢失、骨质破环和关节功能丧失[3]。RA的病情呈进展性,疾病的早期可表现出轻微的骨质破坏,随着病情的发展,骨质破坏不断加重[10]。RA病人如果不能得到早期诊断和干预性治疗,局部骨破坏可以很快发生,最终导致关节结构破坏,强直畸形,功能丧失,甚至残废和全身性的骨质疏松[11]。因此,早期给予RA病人有效的干预治疗有重要的意义。但目前,RA骨破坏机制及如何在早期进行及时有效的治疗仍是学术界需要不断探索的问题。
本实验中,模型组大鼠全身评分明显增高,存在明显的软组织肿胀、骨局部密度降低、骨缺损的情况,并且血清钙、磷含量明显减少,说明造模成功,AA大鼠出现了骨破坏。RA骨破坏可能是多种原因综合导致的, 包括某些炎症因子的作用, 免疫功能异常, 钙调节激素异常, 钙摄入不足等因素[12]。血清钙、磷离子含量作为衡量骨矿化及反映骨形成活性的重要指标,可以间接反映骨组织的代谢情况,血清总钙的测定对骨代谢及钙磷代谢的研究具有重要价值[13]。骨中的钙、磷通过成骨和溶骨作用,不断与细胞外液进行钙磷交换,维持血钙和血磷浓度的相对稳定性。磷可促进骨基质的合成和骨矿物质的沉积,改变骨细胞对钙的摄人,导致骨细胞结构和功能的改变。TNF-α主要来自于RA微环境中的巨噬细胞和滑膜细胞,以及活化的T细胞,它直接调节骨髓中破骨细胞前体的含量并且能通过增强RANK信号通路激活破骨细胞[14],也能在成骨细胞系骨髓干细胞中介导RANKL的表达从而间接影响破骨细胞生成。TNF-α可以介导炎症因子IL-6的产生,有研究指出,RA病人循环系统中IL-6水平与渐进性的关节破坏有关[15]。
关于RA骨破坏的机制,有研究[16]表明,正常骨组织处于成骨细胞导致骨形成和破骨细胞导致骨吸收的动态平衡中。OPG、RANKL、RANK是偶联成骨细胞、基质细胞和破骨细胞分化与活化的3种主要细胞因子,在骨代谢的过程中起十分重要的调节作用[17-18]。破骨细胞是造血源的多核细胞,是主要的骨吸收细胞。这些细胞是骨破坏的主要介质,分布在RA病人的滑膜上,并在RA的骨上极化。巨噬细胞驱动的破骨细胞形成需要巨噬细胞集落刺激因子(MCSF)的存在,是RANK和RANKL相互作用的结果[13]。OPG-RANKL-RANK系统是骨代谢的重要环节,在破骨细胞的细胞表面,RANKL可以与RANK的受体激活因子结合,诱导破骨细胞分化、激活和存活。OPG是RANKL的竞争性抑制剂,能够抑制破骨细胞的分化。我们可以通过调节该系统,延缓骨质破坏,从而控制RA骨破坏的病程进展。
二甲双胍作为经典一线降糖药,安全、便宜,不良反应少。除了可以作为降糖药,它还具有抗炎、抗肿瘤、治疗多囊卵巢综合征、调节代谢等作用。同时,它还可以激活AMPK信号通路,是AMPK的激活剂。AMPK是哺乳动物体内一种丝氨酸/苏氨酸激酶,是体内能量代谢至关重要的调节因子,AMPK的激活与TNF-α、IL-6等各种炎症因子表达水平之间存在关联。同时,AMPK信号通路的激活可能是破骨细胞、RANKL和各种细胞因子之间的关键联系。
通过本实验可知,二甲双胍可以改善AA大鼠的炎症反应,改善骨缺损,且与剂量相关。高剂量组血清钙磷水平的变化表明,二甲双胍可以影响骨质疏松大鼠血清钙磷水平,二甲双胍促进OPG的合成,降低RANKL的表达,并且呈浓度依赖关系。对骨的矿化过程、骨代谢的平衡维持也有一定的调节作用,对RA骨破坏起到改善作用。本实验免疫组化结果表明,二甲双胍作为AMPK的激活剂,高中剂量能增加AA大鼠关节组织中的AMPK水平,降低炎症因子TNF-α水平,且各剂量组均可降低IL-6水平。二甲双胍通过激活AMPK信号通路,抑制炎症因子的产生,促进OPG的合成,降低RANKL的表达,从而影响OPG-RANKL-RANK系统,达到治疗RA及其骨破坏的作用。这可能是二甲双胍治疗RA骨破坏的机制之一。
综上所述,二甲双胍可以改善AA大鼠的炎症症状,调节RA骨代谢,对骨破坏起到保护作用,且与剂量相关。作用机制可能与其抗炎、调节血清骨代谢指标及激活AMPK信号通路影响OPG-RANKL-RANK系统相关。二甲双胍作为一线降糖药物对于糖尿病的治疗早已得到肯定。随着研究的深入,它在骨破坏方面的影响得到了广泛关注,但大多集中于糖尿病病人骨质疏松或仅仅研究其对RA的作用。这种潜在的骨保护作用是否会改善由RA引起的骨破坏及其机制如何,这是我们正在探索的内容。虽然二甲双胍的一些促成骨机制仍不十分明确,但相信经过更多的探讨及大量的临床对照研究,二甲双胍将在各种骨破坏缺损相关疾病的治疗中发挥巨大的作用。目前,虽然二甲双胍作用于骨破坏中的研究取得了一些进展,但是其中的作用机制尚需进一步深入探索。在本课题组后续的工作中,将进一步完善二甲双胍作用于体外及RA病人骨破坏相关实验,为临床治疗提供依据。
二甲双胍改善佐剂性关节炎大鼠骨破坏的作用和机制研究
Study on the effects and mechanism of metformin on bone destruction induced by adjuvant arthritis in rats
-
摘要:
目的探讨二甲双胍治疗类风湿性关节炎(rheumatoidrthritis arthritis,RA)骨破坏的作用及机制。 方法采用Freund完全佐剂诱导佐剂性关节炎(adjuvant arthritis,AA)大鼠模型。全身评分评价不同剂量二甲双胍对AA大鼠炎症的作用;对各组大鼠踝关节和足部通过X射线成像进行检查;ELISA法对大鼠外周血中钙离子、磷离子、骨保护素(OPG)、核因子κB受体活化因子配体(RANKL)等指标进行测定;免疫组织化学法测定大鼠膝关节腺苷酸活化蛋白激酶(AMP-activated protein kinase,AMPK)、白细胞介素-6(IL-6)、肿瘤坏死因子α(TNF-α)蛋白表达。探讨二甲双胍对AA大鼠骨破坏的影响及机制。 结果二甲双胍可以改善AA大鼠的全身炎症反应,减轻足爪部肿胀,尤其是高剂量效果更明显。二甲双胍各剂量组均可明显改善AA大鼠的局部骨密度降低和骨缺损;二甲双胍高剂量组血清钙、磷离子水平升高;不同剂量的二甲双胍均可以提高血清OPG,降低RANKL的水平;与模型组相比,二甲双胍可增加AMPK蛋白表达,降低IL-6、TNF-α蛋白表达,以上差异均有统计学意义(P<0.05~P<0.01)。 结论二甲双胍可对RA骨破坏起到保护作用;作用机制可能与其抗炎、调节血清骨代谢指标及激活AMPK信号通路影响OPG-RANKL-RANK系统相关。 Abstract:ObjectiveTo investigate the effects and mechanism of metformin on bone destruction in rheumatoid arthritis(RA). MethodsThe adjuvant arthritis(AA) models with complete Freund's adjuvant(CFA) were established in rats.The systemic inflammation score was used to evaluate the effects of different doses of metformin on inflammation in AA rats; the ankle and foot of each group were examined using X-ray imaging; ELISA was used to measure the serum calcium, phosphorus, osteoprotectin(OPG), nuclear factor κB receptor activator ligand(RANKL) in peripheral blood of rats; the expression levels of AMP-activated protein kinase(AMPK), interleukin-6(IL-6) and tumor necrosis factor α(TNF-α) were measured by immunohistochemistry.The effects of metformin on bone destruction in rats was evaluated. ResultsMetformin could improve the systemic inflammatory response, and reduce paw swelling in AA rats, especially at high dose.All dose metformin groups could significantly improve the local bone mineral density and bone destruction in AA rats.The serum levels of calcium and phosphorus ion increased in high-dose metformin group.Different doses of metformin could increase the serum OPG level, and decrease the serum RANKL level.Compared with the model group, metformin could increase the protein expression of AMPK, decrease the protein expression of IL-6 and TNF-α, and the differences of which were statistically significant(P<0.05 to P<0.01). ConclusionsMetformin plays a protective role on the bone destruction of RA.The mechanism of action may be related to the effects of anti-inflammation, regulation of serum bone metabolism index and activation of AMPK signaling pathway to affect the OPG-RANKL-RANK system. -
Key words:
- rheumatoid arthritis /
- bone destruction /
- metformin /
- rat
-
表 1 各组大鼠全身评分的变化(x±s;分)
分组 n 14 d 17 d 21 d 24 d 27 d 30 d 模型组 8 1.25±0.46 7.50±0.53 7.63±0.52 7.25±0.46 7.13±0.64 5.88±0.64 MTX组 8 1.13±0.35 6.13±0.64** 5.13±0.64** 4.75±0.46** 4.13±0.83** 3.25±0.71** 药物高剂量组 8 1.25±0.46 6.50±0.93** 4.75±0.71** 4.50±0.53** 4.00±0.53** 3.50±0.53** 药物中剂量组 8 1.25±0.49 6.00±0.98** 5.25±0.79** 4.63±0.53** 4.13±0.38** 3.88±0.49** 药物低剂量组 8 1.25±0.46 6.63±0.92* 6.00±0.76** 5.50±0.53** 5.25±0.71** 5.13±0.64** F — 0.12 4.14 21.93 41.32 34.95 27.65 P — >0.05 <0.01 <0.01 <0.01 <0.01 <0.01 MS组内 — 0.200 0.672 0.477 0.253 0.406 0.369 q检验:与模型组比较*P < 0.05, **P < 0.01 表 2 各组大鼠血清骨代谢相关指标水平的比较(x±s)
分组 n 钙/(mmol/L) 磷/(mmol/L) OPG/ (pg/mL) RANKL/(pg/mL) 正常组 8 2.7±0.07 2.39±0.09 1 853.97±184.12 9.86±0.98 模型组 8 2.46±0.05## 2.05±0.06## 623.39±92.72## 20.65±1.59## MTX组 8 2.63±0.08** 2.21±0.09** 1 357.45±146.49** 10.46±1.23** 药物高剂量组 8 2.61±0.05** 2.18±0.08** 1 333.12±80.65** 10.45±1.83** 药物中剂量组 8 2.56±0.07 2.13±0.1 1 001.88±69.65** 14.28±0.78** 药物低剂量组 8 2.48±0.09 2.1±0.07 840.78±56.41** 16.21±0.79** F — 13.87 16.52 118.0 90.89 P — < 0.01 < 0.01 < 0.01 < 0.01 MS组内 — 0.005 0.007 13 082.354 1.597 q检验:与正常组比较##P < 0.01;与模型组比较**P < 0.01 表 3 各组免疫组化结果(AMPK、IL-6、TNF-α)半定量分析(x±s)
分组 n AMPK IL-6 TNF-a 正常组 8 53.29±9.9 40.44±9.16 95.17±15.07 模型组 8 23.88±5.82## 501.52±86.14## 168.16±23.24## MTX组 8 48.65±4.69** 55.40±9.95** 115.96±10.55** 药物高剂量组 8 47.21±3.36** 54.31±13.46** 116.37±15.12** 药物中剂量组 8 40.71±3.69** 134.07±19.83** 124.37±24.26** 药物低剂量组 8 32.85±7.36 166.96±28.79** 149.27±21.45 F — 25.04 163.9 15.30 P — < 0.01 < 0.01 < 0.01 MS组内 — 38.826 1 501.000 359.300 q检验:与正常组比较##P < 0.01;与模型组比较**P < 0.01 -
[1] CHANG Y, JIA X, WEI F, et al. CP-25, a novel compound, protects against autoimmune arthritis by modulating immune mediators of inflammation and bone damage[J]. Sci Rep, 2016, 6: 26239. doi: 10.1038/srep26239 [2] WANG X, HE X, ZHANG CF, et al. Anti-arthritic effect of berberine on adjuvant-induced rheumatoid arthritis in rats[J]. Biomed Pharmacother, 2017, 89: 887. doi: 10.1016/j.biopha.2017.02.099 [3] XIE J, LI S, XIAO L, et al. Zoledronic acid ameliorates the effects of secondary osteoporosis in rheumatoid arthritis patients[J]. J Orthop Surg Res, 2019, 14(1): 421. doi: 10.1186/s13018-019-1492-3 [4] ONO Y, MIYAKOSHI N, KASUKAWA Y, et al. Micro-CT imaging analysis for the effects of ibandronate and eldecalcitol on secondary osteoporosis and arthritis in adjuvant-induced arthritis rats[J]. Biomed Res, 2019, 40(5): 197. doi: 10.2220/biomedres.40.197 [5] LORENZO J, HOROWITZ M, CHOI Y. Osteoimmunology: interactions of the bone and immune system[J]. Endocr Rev, 2008, 29(4): 403. [6] SOKKA T, PINCUS T. Eligibility of patients in routine care for major clinical trials of anti-tumor necrosis factor alpha agents in rheumatoid arthritis[J]. Arthritis Rheum, 2003, 48(2): 313. doi: 10.1002/art.10817 [7] MCCARTHY AD, CORTIZO AM, SEDLINSKY C. Metformin revisited: Does this regulator of AMP-activated protein kinase secondarily affect bone metabolism and prevent diabetic osteopathy[J]. World J Diabetes, 2016, 7(6): 122. doi: 10.4239/wjd.v7.i6.122 [8] HYUN B, SHIN S, LEE A, et al. Metformin Down-regulates TNF-α Secretion via Suppression of Scavenger Receptors in Macrophages[J]. Immune Netw, 2013, 13(4): 123. doi: 10.4110/in.2013.13.4.123 [9] WANG D, CHANG Y, WU Y, et al. Therapeutic effects of TACI-Ig on rat with adjuvant arthritis[J]. Clin Exp Immunol, 2011, 163(2): 225. doi: 10.1111/j.1365-2249.2010.04293.x [10] IWAMOTO J, SATO Y, UZAWA M, et al. Seven years' experience with alendronate in postmenopausal Japanese women with osteoporosis[J]. Ther Clin Risk Manag, 2010, 6: 201. [11] 杜欢, 许霞. 近5年来类风湿关节炎发病机制研究进展[J]. 辽宁中医药大学学报, 2015, 17(10): 77. [12] FIRESTEIN GS, MCINNES IB. Immunopathogenesis of Rheumatoid Arthritis[J]. Immunity, 2017, 46(2): 183. doi: 10.1016/j.immuni.2017.02.006 [13] GRIZ L, FONTAN D, MESQUITA P, et al. Diagnosis and management of Paget's disease of bone[J]. Arq Bras Endocrinol Metabol, 2014, 58(6): 587. doi: 10.1590/0004-2730000002941 [14] HASEGAWA T, KIKUTA J, SUDO T, et al. Identification of a novel arthritis-associated osteoclast precursor macrophage regulated by FoxM1[J]. Nat Immunol, 2019, 20(12): 1631. doi: 10.1038/s41590-019-0526-7 [15] SALVATORE T, PAFUNDI PC, GALIERO R, et al. Metformin: a potential therapeutic tool for rheumatologists[J]. Pharmaceuticals (Basel), 2020, 13(9): 234. doi: 10.3390/ph13090234 [16] TAKAYANAGI H. New developments in osteoimmunology[J]. Nat Rev Rheumatol, 2012, 8(11): 684. doi: 10.1038/nrrheum.2012.167 [17] TANAKA S, TANAKA Y, ISHIGURO N, et al. RANKL: A therapeutic target for bone destruction in rheumatoid arthritis[J]. Mod Rheumatol, 2018, 28(1): 9. [18] ZHAO J, LI Y, ZHANG H, et al. Preventative effects of metformin on glucocorticoid-induced osteoporosis in rats[J]. J Bone Miner Metab, 2019, 37(5): 805. -




 下载:
下载:






