-
子宫内膜癌(endometrial cancer,EC)是一种女性生殖系统最常见的上皮性恶性肿瘤,于围绝经期以及绝经妇女最为常见,EC发病率不断升高并年轻化[1]。寻找新的分子靶向标志物有助于EC诊疗。miRNA为小分子非编码RNA,参与细胞的增殖、转移等恶性生物学进程。研究[2]显示,miR-367促进了髓母细胞瘤细胞的增殖和侵袭。miR-367通过靶向Smad7-TGF-β信号通路促进胰腺导管腺癌细胞的上皮向间充质转化和侵袭[3]。miR-367可能通过抑制KLF4促进乳腺癌MCF-7细胞的增殖、迁移和侵袭[4]。但是miR-367在EC中的作用鲜有报道。10-11异位的甲基胞嘧啶双加氧酶2(ten-eleven translocation methylcytosine dioxygenase 2,TET2)属于TET蛋白家族成员之一,主要在造血系统中高表达。有研究[5]表明,TET2蛋白在膀胱癌细胞T739中低表达。在乳腺癌细胞中,赖氨酸脱甲基酶2A(KDM2A)通过抑制TET2表达从而促进乳腺癌细胞的增殖[6]。本研究探讨miR-367与TET2的相互关系,观察其对EC细胞恶性增殖的影响。
-
人EC HEC-1A细胞(货号:CL0131)购自丰晖生物。
-
RPMI 1640培养基(货号:11875-093)、胎牛血清(货号:10270-106)、胰蛋白酶(货号:12605036)均购自美国Gibco;脂质体LipofectamineTM2000(货号:11668027)购自美国Invitrogen;MTT试剂盒(货号:M6494)购自美国ThermoFisher公司;Transwell小室、基质胶(货号:354480)购自美国BD;RevertAid First Strand cDNA Synthesis Kit(货号:K1622)购自德国Thermo Scientific;TET2抗体(货号:18950)购自美国Cell signaling Technology;兔抗人c-Myc(货号:MAB3696)、兔抗人CyclinD1(货号:MAB4314))购于美国R & DSYSTEMS;兔抗人MMP-2(货号:ab92536)、MMP-9(货号:ab228402)购自美国Abcam公司;GAPDH抗体购自北京全式金有限公司;辣根过氧化物酶标记山羊抗兔IgG(货号:711-035-152)抗体购自美国杰克逊免疫研究实验室。
-
将冷藏在液氮罐中的HEC-1A细胞,37 ℃水浴1~2 min。待细胞完全溶解后,700 g离心4 min,将细胞沉淀用含10%胎牛血清的RPMI 1640培养基培养,于5% CO2、37 ℃、饱和湿度培养箱中常规培养。待细胞融合至90%以上时胰酶消化,并进行后续研究。
-
取对数期的HEC-1A细胞消化,以1×106细胞/孔接种到24孔板中,37 ℃培养箱培养,细胞密度达50%时,使用脂质体LipofectamineTM2000将mimics NC或miR-367 mimics、inhibitor NC、miR-367 inhibitor分别转染HEC-1A细胞,分别将脂质体混合物加入到24孔板中。
将HEC-1A细胞分为5组:空白组(NG)、阴性转染组(mimics NC)、miR-367过表达组(miR-367 mimics)、inhibitor NC、miR-367 inhibitor,序列由上海生工设计并合成。
-
提取各组细胞总RNA,进行反转录成cDNA,以GAPDH为内参。反应体系:上下游分别加入1 μL,模板加入2 μL,荧光MIX SYBR Premix Ex TapTM(2×)加入8 μL,用水补足到20 μL。反应程序:95 ℃预变性10 min,94 ℃变性10 s,58 ℃退火25 s,72 ℃延伸30 s,共40个循环,然后72 ℃延伸10 min。所用引物见表 1。每组设置6个复孔,实验重复3次,最后求其平均值。采用2-ΔΔCt法计算miR-367、TET2 mRNA水平。
基因 正向引物 反向引物 miR-367 5′-ACT GCA AGA AAC GGT TTT CCC-3′ 5′-GGC GCG GAA CAC TGA GAT GT-3′ TET2 5′-TTC CGC ACA GAC CTC TAA-3′ 5′-TGG TTC CCT GGA TGT TAT-3′ GAPDH 5′-AGA AGGC TGG GGC TCA TTT G-3′ 5′-GCA GGA GGC ATT GCT GAT GAT-3′ U6 5′-TGC GGG TGC TCG CTT CGG CAG C-3′ 5′-CCA GTG CAG GGT CCG AGG T-3′ 表 1 引物序列
-
取各组细胞,调整细胞密度为1×104个/孔接种于96孔板中,分别在转染0、12、24、48 h后,按照MTT试剂盒说明书进行操作,全自动酶标仪检测490 nm波长下各孔细胞吸光值(optical density,OD)。细胞存活率=实验组OD值/空白对照组OD值×100%。
-
收集各组细胞,将细胞密度调整至2×105/mL,添加200 μL细胞液加入包含基质胶的Transwell小室的上室(迁移不需要Matrigel基质胶),用RPMI 1640培养液添加至1 mL,下室加入600 μL完全培养基。培养48 h,擦拭未过膜的细胞,置于4%多聚甲醛中固定20 min,晾干,用1%结晶紫染液浸染20 min,晾干后通过光学显微镜下观察侵袭和迁移细胞。
-
TargetScan软件分析显示miR-367与TET2 3′端上存在结合位点。由广州锐博构建TET2-1-Wt和TET2-Mut载体。将TET2-1-Wt、TET2-Mut与miR-367mimics、mimics NC分别转染至HEC-1A细胞。48 h后采用检测试剂盒测定细胞相对荧光素酶活性。
-
RIPA裂解液提取各组细胞总蛋白,采用BCA蛋白试剂盒对细胞中总蛋白进行定量,用SDS-PAGE分离蛋白,湿转法将蛋白转移至PVDF膜上,5%脱脂牛奶封闭1 h,在4 ℃冰箱过夜孵育一抗TET2(1∶ 200)、c-myc(1∶ 500)、cyclin D1(1∶ 500)、MMP-2(1∶ 1 000)、MMP-9(1∶ 500)、GAPDH(1∶ 500)过夜,用TBST洗涤后加入二抗(1∶ 5 000)常温下孵育2 h。采用蛋白成像凝胶仪对TET2、c-myc、cyclin D1、MMP-2、MMP-9蛋白水平进行半定量分析。每组设置6个复孔,实验重复3次。
-
采用方差分析和q检验。
-
与NG、mimics NC组相比,miR-367 mimics组TET2 mRNA表达水平均下降(P < 0.05),miR-367表达水平均升高(P < 0.05);与NG、inhibitor NC组相比,miR-367 inhibitor组TET2 mRNA表达水平均升高(P < 0.05),miR-367表达水平均下降(P < 0.05)(见表 2)。
分组 TET2 miR-367 NG组 1.00±0.00 1.00±0.00 mimics NC组 1.08±0.16 1.12±0.17 miR-367 mimics组 0.66±0.06*# 1.69±0.28*# inhibitor NC组 1.18±0.17 1.22±0.16 miR-367 inhibitor组 1.78±0.18*■ 0.56±0.07*■ F 55.09 36.08 P < 0.01 < 0.01 MS组内 0.018 0.028 q检验:与NG组比较*P < 0.05;与mimics NC组比较#P < 0.05;与inhibitor NC组比较■P < 0.05 表 2 各组HEC-1A细胞miR-367、TET2 mRNA表达水平比较(ni=6;x±s)
-
与NG、mimics NC组相比,24、48 h时miR-367 mimics组细胞存活率均上升(P < 0.05);与NG、inhibitor NC组相比,24、48 h时miR-367 inhibitor组细胞存活率均降低(P < 0.05)(见表 3)。
分组 细胞存活率/% 12 h 24 h 48 h NG组 100 100 100 mimics NC组 103.23±14.41 107.36±12.36 102.31±15.69 miR-367 mimics组 101.52±12.58 162.35±17.37*# 191.23±19.79*# inhibitor NC组 102.31±13.07 110.16±12.36 114.21±15.69 miR-367 inhibitor组 103.15±12.9 78.23±7.96*■ 88.42±8.74*■ F 0.07 43.84 52.91 P >0.05 < 00.01 < 00.01 MS组内 175.785 167.654 240.096 q检验:与NG组比较*P < 0.05;与mimics NC组比较#P < 0.05;与inhibitor NC组比较■P < 0.05 表 3 各组HEC-1A细胞增殖水平比较(ni=6;x±s)
-
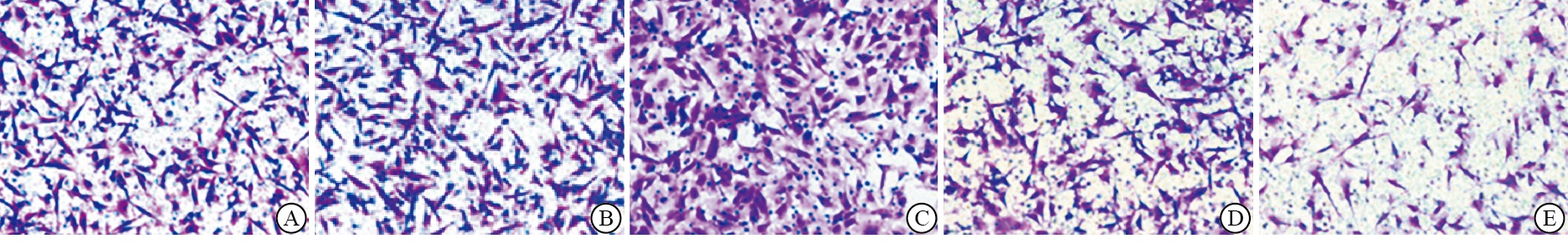
与NG、mimics NC组相比,miR-367 mimics组细胞侵袭、迁移细胞数及MMP-2、MMP-9蛋白表达水平均升高(P < 0.05);与NG、inhibitor NC组相比,miR-367 inhibitor组细胞侵袭、迁移细胞数及MMP-2、MMP-9蛋白表达水平均降低(P < 0.05)(见图 1~3、表 4)。
分组 侵袭细胞数/个 迁移细胞数/个 MMP-2/GAPDH MMP-9/GAPDH NG组 142.60±25.02 125.66±13.37 1.02±0.12 0.97±0.12 mimics NC组 143.00±25.13 126.12±13.43 0.98±0.11 1.01±0.14 miR-367 mimics组 179.58±17.26*# 155.23±15.16*# 1.56±0.06*# 1.61±0.04*# inhibitor NC组 138.78±15.32 125.31±13.51 1.12±0.14 1.01±0.13 miR-367 inhibitor组 88.78±10.27*■ 107.78±12.37*■ 0.78±0.17*■ 0.59±0.13*■ F 16.60 9.46 31.95 57.72 P < 0.01 < 0.01 < 0.01 < 0.01 MS组内 379.120 184.900 0.015 0.014 q检验:与NG组比较*P < 0.05;与mimics NC组比较#P < 0.05;与inhibitor NC组比较■P < 0.05 表 4 各组HEC-1A细胞侵袭、迁移及相关蛋白表达比较(ni=6;x±s)
-
与NG、mimics NC组相比,miR-367 mimics组TET2蛋白表达水平均降低(P < 0.05),c-myc、cyclin D1蛋白表达水平均升高(P < 0.05);与NG、inhibitor NC组相比,miR-367 inhibitor组TET2蛋白表达水平均升高(P < 0.05),c-myc、cyclin D1蛋白表达水平均降低(P < 0.05)(见图 4、表 5)。
分组 TET2/GAPDH c-myc/GAPDH cyclin D1/GAPDH NG组 1.93±0.36 1.31±0.52 1.16±0.22 mimics NC组 1.92±0.24 1.33±0.53 1.15±0.21 miR-367 mimics组 0.82±0.11*# 1.71±0.27*# 1.85±0.19*# inhibitor NC组 1.94±0.26 1.36±0.23 1.11±0.12 miR-367 inhibitor组 2.13±0.27*■ 0.73±0.07*■ 0.78±0.09*■ F 24.426 5.464 30.308 P < 0.01 < 0.01 < 0.01 MS组内 0.068 0.136 0.030 q检验:与NG组比较*P < 0.05;与mimics NC组比较#P < 0.05;与inhibitor NC组比较■P < 0.05 表 5 各组HEC-1A细胞TET2、c-myc、cyclin D1蛋白表达比较(ni=6;x±s)
-
TargetScan数据库预测结果显示,miR-367在TET2 mRNA 3′UTR有相应的结合位点。荧光素酶报告实验结果显示,miR-367 mimics+WT组HEC-1A细胞荧光素酶活性低于miR-367 NC+WT组(P < 0.05),miR-367 NC+MUT组与miR-367 mimics+MUT组荧光素酶活性差异无统计学意义(P>0.05)(见表 6)。
分组 相对荧光素酶活性 miR-367 NC+WT组 1.02±0.16 miR-367 NC+MUT组 1.03±0.16 miR-367 mimics+WT组 0.57±0.08* miR-367 mimics+MUT组 1.01±0.15 F 15.19 P < 0.01 MS组内 0.020 q检验:与miR-367 NC+WT组比较*P < 0.05 表 6 (ni=6;x±s)
-
EC是一种发生于子宫内膜上皮的恶性肿瘤,发病率较宫颈癌略低,是全球三大常见的妇科恶性肿瘤之一[7]。目前有种类繁多的治疗手段应对EC的扩散,但探究新的靶向治疗位点以提高EC治疗效果,使病人从中获益仍有其研究价值。
miR-367是位于染色体4p25上的一种miRNA,属于miRNA-302/367簇[8],已有的研究[9]主要关注miR-367在胚胎干细胞自我更新和维持多潜能方面的功能。miR-367参与在各种类型的癌症发生,在肝细胞癌[10]、髓母细胞瘤[11]、胰腺癌[12]、非小细胞肺癌[13]和骨肉瘤[14]中发挥促癌作用。相反,在胃癌中,miR-367抑制细胞迁移和侵袭,其在癌组织中的表达远低于正常胃组织[15]。这提示miR-367在不同肿瘤中可能发挥不同的作用。本研究通过转染miR-367 mimics过表达质粒发现,细胞存活率上升,细胞侵袭、迁移细胞数及c-myc、cyclin D1、MMP-2、MMP-9蛋白表达升高;而转染miR-367 inhibitor组细胞存活率降低,细胞侵袭、迁移细胞数及c-myc、cyclin D1、MMP-2、MMP-9蛋白表达降低;说明上调miR-367表达可促进HEC-1A细胞增殖、侵袭与迁移,而下调miR-367表达抑制HEC-1A细胞增殖、侵袭与迁移。
TET2基因是TET基因家族中的一员,TET2酶活性可催化DNA的5mC转化为5hmC,从而使DNA去甲基化[16]。研究[17]表明,TET2基因沉默与造血系统恶性肿瘤的发生有着密切相关,此外在乳腺癌[18]、前列腺癌[19]、卵巢癌[20]等恶性肿瘤中低表达。已有研究[21]表明,Zfp281的直接转录靶标miR-302/367负向调控TET2的表达,从而建立并维持了多能性。本研究经软件预测miR-367靶基因,最终将TET2作为研究对象。双荧光素酶报告基因实验发现,miR-367可抑制野生型TET2组荧光素酶活性,TET2基因3′UTR区与miR-367结合位点发生突变可以恢复荧光素酶活性,提示TET2可靶向调控miR-367基因。且过表达miR-367可显著抑制HEC-1A细胞TET2蛋白表达,表明在HEC-1A细胞中,过表达miR-367可能通过抑制TET2基因表参与促进细胞侵袭和迁移进程。
综上所述,miR-367可促进HEC-1A细胞增殖、侵袭与迁移,可能通过靶向负调控TET2实现的。因此,miR-367可能作为EC治疗潜在靶点。
miR-367通过靶向调控TET2对子宫内膜癌细胞增殖、迁移及侵袭的影响
Effects of miR-367 on proliferation, migration and invasion of endometrial cancer cells by targeted regulating TET2
-
摘要:
目的探讨miR-367通过靶向调控10-11异位的甲基胞嘧啶双加氧酶2(TET2)对子宫内膜癌细胞增殖、迁移及侵袭的影响。 方法将人子宫内膜癌HEC-1A细胞分为5组:空白组(NG)、阴性转染组(mimics NC)、miR-367过表达组(miR-367 mimics)、inhibitor NC组、miR-367 inhibitor组。qRT-PCR检测HEC-1A细胞中TET2 mRNA、miR-367表达水平;MTT法检测细胞增殖情况;Transwell法检测细胞侵袭和迁移能力;TargetScan数据库预测miR-367的靶基因并用双荧光素酶报告基因实验加以验证;Western blotting检测TET2、c-myc、cyclin D1、MMP-2、MMP-9蛋白表达水平。 结果与NG、mimics NC组相比,miR-367 mimics组HEC-1A细胞TET2 mRNA表达水平下降(P < 0.05),miR-367表达水平升高,24、48 h细胞存活率上升,侵袭、迁移细胞数增加(P < 0.05),TET2蛋白表达水平降低(P < 0.05),MMP-2、MMP-9、c-myc、cyclin D1蛋白表达水平升高(P < 0.05)。与NG、inhibitor NC组相比,miR-367 inhibitor组HEC-1A细胞TET2 mRNA表达水平升高(P < 0.05),miR-367表达水平下降,24、48 h细胞存活率降低,侵袭、迁移细胞数减少,TET2蛋白表达水平升高(P < 0.05),MMP-2、MMP-9、c-myc、cyclin D1蛋白表达水平降低(P < 0.05)。TargetScan数据库预测显示miR-367是TET2潜在靶基因。荧光素酶报告实验结果显示,miR-367 mimics+WT组HEC-1A细胞荧光素酶活性低于miR-367 NC+WT组(P < 0.05),miR-367 NC+MUT组与miR-367 mimics+MUT组荧光素酶活性差异无统计学意义(P>0.05)。 结论miR-367过表达可能通过靶向抑制TET2促进子宫内膜癌HEC-1A细胞增殖、迁移和侵袭。 Abstract:Objective To investigate the effect of miR-367 on the proliferation, migration and invasion of endometrial cancer cells by targeted regulating ten-eleven translocation methylcytosine dioxygenase 2(TET2). MethodsHuman endometrial cancer HEC-1A cells were divided into 5 groups: blank group(NG), negative transfection group(mimics NC), miR-367 overexpression group(miR-367 mimics), inhibitor NC group and miR-367 inhibitor group.qRT-PCR was used to determine the expression levels of TET2 mRNA and miR-367 in HEC-1A cells; MTT assay was applied to detect cell proliferation; Transwell assay was carried out to detect cell invasion and migration ability; TargetScan database was employed to predict the target gene of miR-367, and dual luciferase reporter gene assay was used to verify the relationship; Western blotting was performed to analyze the protein expression levels of TET2, c-myc, cyclin D1, MMP-2 and MMP-9. ResultsCompared with the NG group and mimics NC group, in the miR-367 mimics group, the expression level of TET2 mRNA in HEC-1A cells decreased(P < 0.05), the expression level of miR-367 increased(P < 0.05), the cell survival rate aftertreated for 24, 48 h and number of invaded and migrated cells increased(P < 0.05), the protein expression level of TET2 decreased(P < 0.05), the protein expression levels of MMP-2, MMP-9, c-myc and cyclin D1 increased(P < 0.05).Compared with NG group and inhibitor NC group, in the miR-367 inhibitor group, the expression level of TET2 mRNA in HEC-1A cells increased(P < 0.05), the expression level of miR-367 decreased(P < 0.05), the cell survival rate aftertreated for 24, 48 h and number of invaded and migrated cells decreased, the protein expression level of TET2 increased(P < 0.05), the protein expression level of MMP-2, MMP-9, c-myc and cyclin D1 decreased(P < 0.05).TargetScan database prediction showed that miR-367 was a potential target gene of TET2.The results of the luciferase reporter assay showed that the luciferase activity of HEC-1A cells in the miR-367 mimics+WT group was lower than that in the miR-367 NC+WT group(P < 0.05), and there was no significant difference in luciferase activity between the miR-367 NC+MUT group and miR-367 mimics+MUT group(P>0.05). ConclusionsOverexpression of miR-367 may promote the proliferation, migration and invasion of endometrial cancer HEC-1A cells by targeted inhibiting TET2. -
表 1 引物序列
基因 正向引物 反向引物 miR-367 5′-ACT GCA AGA AAC GGT TTT CCC-3′ 5′-GGC GCG GAA CAC TGA GAT GT-3′ TET2 5′-TTC CGC ACA GAC CTC TAA-3′ 5′-TGG TTC CCT GGA TGT TAT-3′ GAPDH 5′-AGA AGGC TGG GGC TCA TTT G-3′ 5′-GCA GGA GGC ATT GCT GAT GAT-3′ U6 5′-TGC GGG TGC TCG CTT CGG CAG C-3′ 5′-CCA GTG CAG GGT CCG AGG T-3′ 表 2 各组HEC-1A细胞miR-367、TET2 mRNA表达水平比较(ni=6;x±s)
分组 TET2 miR-367 NG组 1.00±0.00 1.00±0.00 mimics NC组 1.08±0.16 1.12±0.17 miR-367 mimics组 0.66±0.06*# 1.69±0.28*# inhibitor NC组 1.18±0.17 1.22±0.16 miR-367 inhibitor组 1.78±0.18*■ 0.56±0.07*■ F 55.09 36.08 P < 0.01 < 0.01 MS组内 0.018 0.028 q检验:与NG组比较*P < 0.05;与mimics NC组比较#P < 0.05;与inhibitor NC组比较■P < 0.05 表 3 各组HEC-1A细胞增殖水平比较(ni=6;x±s)
分组 细胞存活率/% 12 h 24 h 48 h NG组 100 100 100 mimics NC组 103.23±14.41 107.36±12.36 102.31±15.69 miR-367 mimics组 101.52±12.58 162.35±17.37*# 191.23±19.79*# inhibitor NC组 102.31±13.07 110.16±12.36 114.21±15.69 miR-367 inhibitor组 103.15±12.9 78.23±7.96*■ 88.42±8.74*■ F 0.07 43.84 52.91 P >0.05 < 00.01 < 00.01 MS组内 175.785 167.654 240.096 q检验:与NG组比较*P < 0.05;与mimics NC组比较#P < 0.05;与inhibitor NC组比较■P < 0.05 表 4 各组HEC-1A细胞侵袭、迁移及相关蛋白表达比较(ni=6;x±s)
分组 侵袭细胞数/个 迁移细胞数/个 MMP-2/GAPDH MMP-9/GAPDH NG组 142.60±25.02 125.66±13.37 1.02±0.12 0.97±0.12 mimics NC组 143.00±25.13 126.12±13.43 0.98±0.11 1.01±0.14 miR-367 mimics组 179.58±17.26*# 155.23±15.16*# 1.56±0.06*# 1.61±0.04*# inhibitor NC组 138.78±15.32 125.31±13.51 1.12±0.14 1.01±0.13 miR-367 inhibitor组 88.78±10.27*■ 107.78±12.37*■ 0.78±0.17*■ 0.59±0.13*■ F 16.60 9.46 31.95 57.72 P < 0.01 < 0.01 < 0.01 < 0.01 MS组内 379.120 184.900 0.015 0.014 q检验:与NG组比较*P < 0.05;与mimics NC组比较#P < 0.05;与inhibitor NC组比较■P < 0.05 表 5 各组HEC-1A细胞TET2、c-myc、cyclin D1蛋白表达比较(ni=6;x±s)
分组 TET2/GAPDH c-myc/GAPDH cyclin D1/GAPDH NG组 1.93±0.36 1.31±0.52 1.16±0.22 mimics NC组 1.92±0.24 1.33±0.53 1.15±0.21 miR-367 mimics组 0.82±0.11*# 1.71±0.27*# 1.85±0.19*# inhibitor NC组 1.94±0.26 1.36±0.23 1.11±0.12 miR-367 inhibitor组 2.13±0.27*■ 0.73±0.07*■ 0.78±0.09*■ F 24.426 5.464 30.308 P < 0.01 < 0.01 < 0.01 MS组内 0.068 0.136 0.030 q检验:与NG组比较*P < 0.05;与mimics NC组比较#P < 0.05;与inhibitor NC组比较■P < 0.05 表 6 (ni=6;x±s)
分组 相对荧光素酶活性 miR-367 NC+WT组 1.02±0.16 miR-367 NC+MUT组 1.03±0.16 miR-367 mimics+WT组 0.57±0.08* miR-367 mimics+MUT组 1.01±0.15 F 15.19 P < 0.01 MS组内 0.020 q检验:与miR-367 NC+WT组比较*P < 0.05 -
[1] 王建梅, 王羽, 周宏萍, 等. 人附睾分泌蛋白4, 糖链多肽抗原125联合超声对绝经后子宫内膜癌的诊断价值[J]. 蚌埠医学院学报, 2020, 45(10): 1348. [2] KAID C, SILVA PBG, CORTEZ BA, et al. miR-367 promotes proliferation and stem-like traits in medulloblastoma cells[J]. Cancer Sci, 2015, 106(9): 1188. doi: 10.1111/cas.12733 [3] ZHU Z, XU Y, ZHAO J, et al. miR-367 promotes epithelial-to-mesenchymal transition and invasion of pancreatic ductal adenocarcinoma cells by targeting the Smad7-TGF-β signalling pathway[J]. Br J Cancer, 2015, 112(8): 1367. doi: 10.1038/bjc.2015.102 [4] 周春, 王光华, 张帮柱. miR-367对人乳腺癌MCF-7细胞增殖、侵袭和迁移的影响及其机制[J]. 吉林大学学报(医学版), 2019, 45(6): 1353. [5] 谢梅茂, 王忠军, 胡映秋, 等. TET2蛋白下调5hmC在膀胱癌细胞T739中低表达[J]. 中国医学创新, 2018, 15(8): 36. [6] CHEN JY, LUO CW, LAI YS, et al. Lysine demethylase KDM2A inhibits TET2 to promote DNA methylation and silencing of tumor suppressor genes in breast cancer[J]. Oncogenesis, 2017, 6(8): e369. [7] TORRE LA, BRAY F, SIEGEL RL, et al. Global cancer statistics, 2012[J]. CA Cancer J Clini, 2015, 65(2): 878. [8] GAO Z, ZHU X, DOU Y. The miR-302/367 cluster: a comprehensive update on its evolution and functions[J]. Open Biol, 2015, 5(12): 150138. doi: 10.1098/rsob.150138 [9] MENG X, LU P, FAN Q. miR-367 promotes proliferation and invasion of hepatocellular carcinoma cells by negatively regulating PTEN[J]. Biochem Biophys Res Commun, 2016, 470(1): 187. doi: 10.1016/j.bbrc.2016.01.025 [10] KAID C, SILVA PBG, CORTEZ BA, et al. miR-367 promotes proliferation and stem-like traits in medulloblastoma cells[J]. Cancer Sci, 2015, 106(9): 1188. doi: 10.1111/cas.12733 [11] ZHU Z, XU Y, ZHAO J, et al. miR-367 promotes epithelial-to-mesenchymal transition and invasion of pancreatic ductal adenocarcinoma cells by targeting the Smad7-TGF-β signalling pathway[J]. Br J Cancer, 2015, 112(8): 1367. doi: 10.1038/bjc.2015.102 [12] XIAO GD, GAO X, SUN X, et al. miR-367 promotes tumor growth by inhibiting FBXW7 in NSCLC[J]. Oncol Rep, 2017, 38(2): 1190. doi: 10.3892/or.2017.5755 [13] WANG GC, HE QY, TONG DK, et al. MiR-367 negatively regulates apoptosis induced by adriamycin in osteosarcoma cells by targeting KLF4[J]. J Bone Oncol, 2016, 5(2): 51. doi: 10.1016/j.jbo.2016.02.002 [14] BIN Z, DEDONG H, XIANGJIE F, et al. The microRNA-367 inhibits the invasion and metastasis of gastric cancer by directly repressing Rab23[J]. Genet Test Mol Biomarkers, 2015, 19(2): 69. doi: 10.1089/gtmb.2014.0210 [15] MARLIES M, REINHARD H, ALAIN P, et al. Microbial signals drive pre-leukaemic myeloproliferation in a Tet2-deficient host[J]. Nature, 2018, 557(7706): 580. doi: 10.1038/s41586-018-0125-z [16] 刘心玉, 杨卫平, 景晓乾. TET2蛋白在恶性肿瘤中的调控因素研究进展[J]. 中国药物与临床, 2014, 14(3): 321. [17] YANG L, YU SJ, HONG Q, et al. Reduced expression of TET1, TET2, TET3 and TDG mRNAs are associated with poor prognosis of patients with early breast cancer[J]. PLoS One, 2015, 10(7): e0133896. doi: 10.1371/journal.pone.0133896 [18] KOBOLDT DC, KANCHI KL, GUI B, et al. Rare variation in TET2 is associated with clinically relevant prostate carcinoma in African-Americans[J]. Cancer Epidemiol Biomarkers Prev, 2016, 25(11): 1456. doi: 10.1158/1055-9965.EPI-16-0373 [19] 张秦. microRNA-142-3p对TET2基因的调控及其对卵巢癌细胞SKOV3增殖的影响[J]. 现代妇产科进展, 2016, 25(10): 721. [20] FIDALGO M, HUANG X, GUALLAR D, et al. Zfp281 coordinates opposing functions of Tet1 and Tet2 in pluripotent states[J]. Cell Stem Cell, 2016, 19(3): 355. doi: 10.1016/j.stem.2016.05.025 -





 下载:
下载: