-
慢性心力衰竭(CHF)是指持续存在的心力衰竭状态,可稳定、恶性或出现失代偿[1]。作为心脏疾病的晚期阶段或严重表现,CHF再住院率和病死率居高不下,研究[2]显示,CHF院内死亡率为4.1%,1年再入院率达18.3%[3]。8%~54%的CHF病人由于静息能量消耗增加、肠道水肿和肝脏充血致吸收不良、食欲减退摄入减少、炎症状态等原因合并营养不良[4-5],作为CHF病人不良预后的独立危险因素,营养不良问题逐渐受到重视[6-7]。2项多中心研究[8-9]表明,针对营养不良的病人进行早期营养干预,能有效降低死亡率。CHF病人入院时可能已经合并营养不良或有营养不良的风险,对其进行早期识别, 及时进行干预,对于改善治疗效果尤为重要。研究[10]表明,前白蛋白(PA)是监测住院病人营养不良的敏感标志物,其血清水平与营养状况的早期变化密切相关,并随着营养支持的变化而变化。入院前较低的PA水平是CHF病人住院死亡率的独立预测因素,但在不同研究中,PA的诊断界值变化波动大[11]。本研究探讨PA在CHF病人预后评估中的临床价值,并为确定最佳诊断界值提供参考。
-
选取2019年9月至2021年2月某三级甲等医院心血管内科收治的CHF病人。纳入标准:(1)符合《中国心力衰竭诊断和治疗指南2018》中CHF的诊断标准[12];(2)美国纽约心脏协会(NYHA)心功能分级Ⅱ~Ⅳ级。排除标准:严重的肝肾疾病、甲状腺疾病、恶性肿瘤、严重感染或肺结核、严重营养不良或急性心肌梗死病人。本研究已通过本院伦理委员会伦理审查,伦理号[20-21]3号,病人均知情同意。
-
通过中国CHF中心数据填报平台和我院病历系统,收集研究对象的一般资料、实验室指标、影像学指标(超声心动图)、出入院时间和出院后药物服用情况等信息。入院第2天,清晨空腹静脉采血,测定包括血清PA、白蛋白等实验室指标,采用酶联免疫吸附试验测定氨基末端脑钠肽前体(NT-proBNP)水平;采用超声心动图测定左心室射血分数(LVEF);NYHA心功能分级在入院时进行评估。
-
病人均按《中国心力衰竭诊断和治疗指南2018》进行标准化治疗,按照CHF中心随访要求进行电话或门诊随访,以发生主要心血管不良事件(MACE)为随访观察终点,MACE定义为因心力衰竭症状加重再入院或心血管死亡。根据MACE是否发生,分为MACE组和非MACE组,随访时间至出院后180 d。
-
采用t检验、Mann-Whitney U非参数检验、χ2检验、logistic回归分析、Kaplan-Meier法和log-rank检验,绘制受试者工作特征(ROC)曲线评估PA对MACE的预测能力。
-
本研究共纳入213例病人,随访期内共100例发生MACE,即非MACE组113例,MACE组100例。MACE组体质量、总胆固醇、白蛋白、服用β受体阻滞剂、PA水平均低于非MACE组,服用醛固酮受体阻滞剂、C反应蛋白、NT-proBNP、肌酐和尿酸水平均高于非MACE组(P < 0.05~P < 0.01)(见表 1)。
项目 非MACE组
(n=113)MACE组
(n=100)t P 男 53 58 2.62* >0.05 年龄/岁 69.31±11.79 72.33±11.82 1.86 >0.05 身高/m 1.61±0.10 1.62±0.08 0.74 >0.05 体质量/kg 65.91±13.35 61.79±13.93 2.20 < 0.05 吸烟 31 33 0.78* >0.05 血红蛋白/(g/L) 123.00(113.00, 134.00) 120.00(106.25, 131.75) 1.91# >0.05 总胆固醇/(mmol/L) 3.87±1.02 3.38±0.91 3.64 < 0.01 低密度脂蛋白/(mmol/L) 2.04±0.77 1.86±0.65 1.85 >0.05 白蛋白/(g/L) 36.06±3.42 33.25±3.83 5.66 < 0.01 PA/(mg/L) 219.77±49.91 161.26±46.87 8.79 < 0.01 C反应蛋白/(mg/L) 3.58(1.29, 9.94) 6.96(2.65, 20.59) 3.39# < 0.01 NT-proBNP/(pg/L) 1 841.00(837.50, 4 105.50) 5 992.00(2 643.75, 13 257.00) 6.49# < 0.01 LVEF/% 46.87±12.83 44.40±12.34 1.29 >0.05 肌酐/(μmol/L) 70.10(57.15, 80.60) 77.05(63.48, 96.15) 3.28# < 0.01 尿酸/(μmol/L) 381.31±127.73 438.06±149.47 2.99 < 0.01 高血压 65 49 1.55* >0.05 糖尿病 28 22 0.23* >0.05 NYHA心功能分级 Ⅱ级 35 20 Ⅲ级 69 56 11.51* < 0.01 Ⅳ级 9 24 ACEI/ARB/ARNI 85 71 0.48* >0.05 β受体阻滞剂 82 58 5.00* < 0.05 醛固酮受体阻滞剂 94 94 5.99* < 0.05 *示χ2值;#示Zc值;ACEI为血管紧张素转换酶抑制剂;ARB为血管紧张素Ⅱ受体拮抗剂;ARNI为血管紧张素受体脑啡肽酶抑制剂 表 1 一般资料在2组中的比较(x ± s)
-
以是否发生MACE作为因变量,将表 1中P < 0.05变量(体质量、NYHA心功能分级、服用β受体阻滞剂、服用醛固酮受体阻滞剂、总胆固醇、白蛋白、PA、C反应蛋白、NT-proBNP、肌酐)纳入多因素logistic回归分析,将NYHA分级设置哑变量,以心功能Ⅱ级作为参考类别;变量赋值(NYHAⅡ级=0,Ⅲ级=1,Ⅳ级=2;β受体阻滞剂服用=0,未服用=1;醛固酮受体阻滞剂服用=0,未服用=1;NT-proBNP≤3 284 pg/mL=0,NT-proBNP>3 284 pg/mL=1;非MACE=0,MACE=1),分析方法选择Forward:LR,结果表明,血清PA水平降低和血浆NT-proBNP水平升高是发生心力衰竭再入院或心血管死亡的独立危险因素(P < 0.01)(见表 2)。
变量 B SE Waldχ2 P OR 95%CI PA -0.024 0.004 34.92 < 0.01 0.976 0.968~0.984 NT-ProBNP 1.181 0.337 12.26 < 0.01 3.256 1.681~6.306 常量 3.872 0.817 22.48 < 0.01 48.055 — 表 2 CHF病人预后多因素logistic回归分析
-
将变量PA四分位分组,转换成等级变量进行多因素分析,结果见表 3,54例血清PA≤159.9 mg/L的CHF病人中,非MACE组占24.1%,MACE组占75.9%,随着PA逐渐升高,MACE组人数逐渐降低。模型1校正年龄和体质量后,随着PA水平降低,发生MACE的风险有逐渐增高趋势;模型2在模型1基础上继续校正NT-proBNP后,发生MACE的风险仍有增高趋势(P < 0.01)。PA水平在Q3时是Q4时发生MACE风险的2.610倍,随着PA水平的降低,Q2、Q1分别是Q4的9.316倍、13.215倍。
-
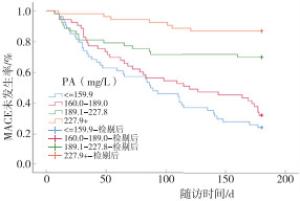
根据不同PA水平对MACE发生率的影响得出Kaplan-Meier曲线图(见图 1),PA水平越低的组,病人MACE发生率越高(χ2=54.18,P < 0.01)。
-
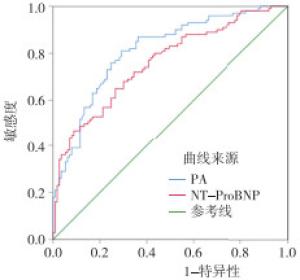
本研究中用PA水平预测MACE发生的ROC曲线下面积为0.810,95%CI: 0.753~0.868,用约登指数最大法计算出最佳临界值PA为191.95 mg/L时灵敏度为81.0%,特异度为70.8%;NT-proBNP的曲线下面积为0.758,95%CI: 0.693~0.822,NT-proBNP最佳临界值为3 649.5 pg/mL时灵敏度为65%,特异度为73.5%(见图 2)。
-
CHF病人不能满足机体的能量需求,心肌底物利用和能量代谢异常,造成合成代谢介质(如胰岛素、生长激素)活性降低,分解代谢介质(如促炎细胞因子、糖皮质激素)活性增加[13],多存在营养不良的风险。未能在住院期间确定病人的营养风险因素可能导致健康恶化、住院时间延长,造成医疗负担[4]。营养管理作为非药物治疗方式,近年来逐渐受到关注,但临床针对CHF病人的营养筛查没有统一的金标准,在难以进行更为详细和全面的营养不良评估环境中,血清PA的测定方便、可行。PA是一种甲状腺激素转运蛋白,以视黄醇结合-PA复合物形式存在于循环系统中,反映了机体氮代谢状态,主要由肝脏合成,部分由肾脏分解代谢,与白蛋白[14]相比,PA的优势主要在于半衰期更短,对营养变化的敏感性更高且不受肠蛋白丢失的影响。中国专家共识[15]指出,应针对CHF病人进行早期准确的营养风险评估,确定积极的肠内肠外营养支持方案,国外营养学会[16]也针对现存证据制定了CHF饮食及营养管理循证实践指南。作为评估营养不良风险的实验室标志物,PA与急性心力衰竭、CHF急性加重、心脏恶病质的预后密切相关[17-18]。本研究中,PA的最佳临界值为191.95 mg/L,是MACE发生的独立预测因子,与鲁敏等[19]研究一致。本研究表明,随着PA水平的降低,MACE发生的风险逐渐增高,在CHF病人临床不良预后评估中呈现递增的附加价值,因此,PA可作为CHF病人营养不良风险早期评估的敏感指标,可针对有风险的病人尽早进行个性化的营养干预。
PA/(mg/L) 非MACE组 MACE组 OR(95%CI) 模型1 模型2 Q1(≤159.9) 13(24.1%) 41(75.9%) 19.134(6.835~53.565) 13.215(4.535~38.502) Q2(160.0~189.0) 17(32.1%) 36(67.9%) 13.277(4.923~35.810) 9.316(3.326~26.088) Q3(189.1~227.8) 37(69.8%) 16(30.2%) 2.750(1.016~7.443) 2.610(0.928~7.343) Q4(≥227.9) 46(86.8%) 7(13.2%) 1.0 1.0 P < 0.01 < 0.01 注:模型1校正年龄、体质量;模型2校正年龄、体质量、NT-proBNP 表 3 PA与发生MACE的趋势性分析
本研究为单中心回顾性研究,尚需要前瞻性研究针对CHF病人进行营养干预后,PA水平的升高与CHF预后的进一步关系。CHF是一种复杂的临床综合征,可能需要联合反映不同营养状况的评分量表评估预后。总之,血清PA水平下降与CHF病人不良预后密切相关,检测PA有利于评估CHF病人预后,指导治疗。
前白蛋白在慢性心力衰竭病人预后评估中的作用
Value of prealbumin in the prognostic evaluation of patients with chronic heart failure
-
摘要:
目的探讨前白蛋白(PA)在慢性心力衰竭(CHF)病人预后评估中的临床价值。 方法CHF病人出院后随访180 d,根据是否发生主要心血管不良事件(MACE)分为MACE组和非MACE组,比较2组一般资料,多因素logistic回归分析发生MACE的影响因素,构建模型验证随着PA的改变发生MACE的趋势性变化,绘制受试者工作特征曲线,确定影响因素的最佳临界值。 结果共纳入213例病人,非MACE组113例,MACE组100例。多因素分析筛选出血清PA降低、血浆氨基末端脑钠肽前体(NT-proBNP)升高为发生MACE的独立危险因素(P < 0.01);经模型1(校正年龄、体质量)、模型2(校正年龄、体质量、NT-proBNP)分析,发生MACE的风险在PA水平上存在趋势(P < 0.01);Kaplan-Meier曲线图显示,PA水平越低,病人MACE发生率越高(P < 0.01);PA为191.95 mg/L时预测MACE发生的受试者工作特征曲线下面积为0.810(95%CI:0.753~0.868)。 结论血清PA水平下降与CHF病人不良预后密切相关。 Abstract:ObjectiveTo explore the clinical value of prealbumin(PA) in the prognostic evaluation of patients with chronic heart failure(CHF). MethodsThe CHF patients were followed up for 180 days after discharge.According to whether major adverse cardiovascular events(MACE) occurred, the patients were divided into the MACE group and non-MACE group.The general data were compared between two groups, and the influencing factors of MACE were analyzed by multivariate logistic regression.A model was built to verify the trend change of MACE with the change of PA, and the receiver operating characteristic curve was drawn to determine the optimal critical value of influencing factors. ResultsA total of 213 patients were enrolled, which included 113 cases in the non-MACE group and 100 cases in the MACE group.The results of multivariate analysis showed that the serum level of PA decreasing and plasma N-terminal pro-B-type natriuretic peptide(NT-proBNP) level increasing were the independent risk factors of MACE(P < 0.01).According to the results of model 1(adjusting the age and body weight) and model 2(adjusting the age, body weight and NT-probNP) analysis, there was a trend in the risk of MACE at PA level(P < 0.01).The results of Kaplan-Meier curve showed that the lower the PA level was, the higher the incidence of MACE was(P < 0.01).When the PA was 191.95 mg/L, the area under the curve predicting MACE incidence was 0.810(95%CI: 0.753-0.868). ConclusionsThe serum level of PA decreasing is closely related to the poor prognosis of CHF patients. -
Key words:
- chronic heart failure /
- prealbumin /
- major adverse cardiovascular events
-
表 1 一般资料在2组中的比较(x ± s)
项目 非MACE组
(n=113)MACE组
(n=100)t P 男 53 58 2.62* >0.05 年龄/岁 69.31±11.79 72.33±11.82 1.86 >0.05 身高/m 1.61±0.10 1.62±0.08 0.74 >0.05 体质量/kg 65.91±13.35 61.79±13.93 2.20 < 0.05 吸烟 31 33 0.78* >0.05 血红蛋白/(g/L) 123.00(113.00, 134.00) 120.00(106.25, 131.75) 1.91# >0.05 总胆固醇/(mmol/L) 3.87±1.02 3.38±0.91 3.64 < 0.01 低密度脂蛋白/(mmol/L) 2.04±0.77 1.86±0.65 1.85 >0.05 白蛋白/(g/L) 36.06±3.42 33.25±3.83 5.66 < 0.01 PA/(mg/L) 219.77±49.91 161.26±46.87 8.79 < 0.01 C反应蛋白/(mg/L) 3.58(1.29, 9.94) 6.96(2.65, 20.59) 3.39# < 0.01 NT-proBNP/(pg/L) 1 841.00(837.50, 4 105.50) 5 992.00(2 643.75, 13 257.00) 6.49# < 0.01 LVEF/% 46.87±12.83 44.40±12.34 1.29 >0.05 肌酐/(μmol/L) 70.10(57.15, 80.60) 77.05(63.48, 96.15) 3.28# < 0.01 尿酸/(μmol/L) 381.31±127.73 438.06±149.47 2.99 < 0.01 高血压 65 49 1.55* >0.05 糖尿病 28 22 0.23* >0.05 NYHA心功能分级 Ⅱ级 35 20 Ⅲ级 69 56 11.51* < 0.01 Ⅳ级 9 24 ACEI/ARB/ARNI 85 71 0.48* >0.05 β受体阻滞剂 82 58 5.00* < 0.05 醛固酮受体阻滞剂 94 94 5.99* < 0.05 *示χ2值;#示Zc值;ACEI为血管紧张素转换酶抑制剂;ARB为血管紧张素Ⅱ受体拮抗剂;ARNI为血管紧张素受体脑啡肽酶抑制剂 表 2 CHF病人预后多因素logistic回归分析
变量 B SE Waldχ2 P OR 95%CI PA -0.024 0.004 34.92 < 0.01 0.976 0.968~0.984 NT-ProBNP 1.181 0.337 12.26 < 0.01 3.256 1.681~6.306 常量 3.872 0.817 22.48 < 0.01 48.055 — 表 3 PA与发生MACE的趋势性分析
PA/(mg/L) 非MACE组 MACE组 OR(95%CI) 模型1 模型2 Q1(≤159.9) 13(24.1%) 41(75.9%) 19.134(6.835~53.565) 13.215(4.535~38.502) Q2(160.0~189.0) 17(32.1%) 36(67.9%) 13.277(4.923~35.810) 9.316(3.326~26.088) Q3(189.1~227.8) 37(69.8%) 16(30.2%) 2.750(1.016~7.443) 2.610(0.928~7.343) Q4(≥227.9) 46(86.8%) 7(13.2%) 1.0 1.0 P < 0.01 < 0.01 注:模型1校正年龄、体质量;模型2校正年龄、体质量、NT-proBNP -
[1] 中华医学会老年医学分会心血管疾病学组, 老年慢性心力衰竭诊治中国专家共识编写组. 老年人慢性心力衰竭诊治中国专家共识(2021)[J]. 中华老年医学杂志, 2021, 40(5): 550. doi: 10.3760/cma.j.issn.0254-9026.2021.05.002 [2] ZHANG Y, ZHANG J, BUTLER J, et al. Contemporary epidemiology, management, and outcomes of patients hospitalized for heart failure in China: results from the China heart failure(China-HF) registry[J]. J CARD FAIL, 2017, 23(12): 868. doi: 10.1016/j.cardfail.2017.09.014 [3] 侯修敏, 张银妆, 匡圆圆, 等. 2013-2016年湘雅医院心力衰竭住院患者的病因、诊治特点及预后影响因素[J]. 临床与病理杂志, 2018, 38(3): 538. [4] VEST AR, CHAN M, DESWAL A, et al. Nutrition, obesity, and cachexia in patients with heart failure: a consensus statement from the Heart Failure Society of America Scientific Statements Committee[J]. J Card Fail, 2019, 25(5): 380. doi: 10.1016/j.cardfail.2019.03.007 [5] YIN J, LU X, QIAN Z, et al. New insights into the pathogenesis and treatment of sarcopenia in chronic heart failure[J]. Theranostics, 2019, 9(14): 4019. doi: 10.7150/thno.33000 [6] GASTELURRUTIA P, LUPON J, DE AM, et al. Body mass index, body fat, and nutritional status of patients with heart failure: the PLICA study[J]. Clinn Nutr, 2015, 34(6): 1233. doi: 10.1016/j.clnu.2014.12.013 [7] SCIATTI E, LOMBARDI C, RAVERA A, et al. Nutritional deficiency in patients with heart failure[J]. Nutrients, 2016, 8(7): 442. doi: 10.3390/nu8070442 [8] DEUTZ NE, MATHESON EM, MATARESE LE, et al. Readmission and mortality in malnourished, older, hospitalized adults treated with a specialized oral nutritional supplement: a randomized clinical trial[J]. Clin Nutr, 2016, 35(1): 18. doi: 10.1016/j.clnu.2015.12.010 [9] SCHUETZ P, FEHR R, BAECHLI V, et al. Individualised nutritional support in medical inpatients at nutritional risk: a randomised clinical trial[J]. Lancet, 2019, 393(10188): 2312. doi: 10.1016/S0140-6736(18)32776-4 [10] DEVOTO G, GALLO F, MARCHELLO C, et al. Prealbumin serum concentrations as a useful tool in the assessment of malnutrition in hospitalized patients[J]. Clin Chem, 2006, 52(12): 2281. doi: 10.1373/clinchem.2006.080366 [11] FOIN N, ALEGRIA E, SEN S, et al. Importance of knowing stent design threshold diameters and post-dilatation capacities to optimise stent selection and prevent stent overexpansion/incomplete apposition during PCI[J]. Int J Cardiol, 2013, 166(3): 755. doi: 10.1016/j.ijcard.2012.09.170 [12] 中华医学会心血管病学分会心力衰竭学组, 中国医师协会心力衰竭专业委员会, 中华心血管痛杂志编辑委员会. 中国心力衰竭诊断和治疗指南2018[J]. 中华心血管病杂志, 2018, 46(10): 760. doi: 10.3760/cma.j.issn.0253-3758.2018.10.004 [13] BILLINGSLEY HE, HUMMEL SL, CARBONE S. The role of diet and nutrition in heart failure: a state-of-the-art narrative review[J]. Prog Cardiovasc Dis, 2020, 63(5): 538. doi: 10.1016/j.pcad.2020.08.004 [14] KELLER U. Nutritional laboratory markers in malnutrition[J]. J Clin Med, 2019, 8(6): 775. doi: 10.3390/jcm8060775 [15] 常翠青, 赵文华, 贾梅. 心血管疾病营养处方专家共识[J]. 中华内科杂志, 2014, 53(2): 151. [16] KUEHNEMAN T, GREGORY M, DE WD, et al. Academy of nutrition and dietetics evidence-based practice guideline for the management of heart failure in adults[J]. J Acad Nutr Diet, 2018, 118(12): 2331. doi: 10.1016/j.jand.2018.03.004 [17] YAMADA T, HARUKI S, MINAMI Y, et al. The C-reactive protein to prealbumin ratio on admission and its relationship with outcome in patients hospitalized for acute heart failure[J]. J Cardiol, 2021, 78(4): 308. doi: 10.1016/j.jjcc.2021.05.009 [18] ARAUJO JP, LOURENCO P, ROCHA GF, et al. Nutritional markers and prognosis in cardiac cachexia[J]. Int J Cardiol, 2011, 146(3): 359. [19] 鲁敏, 孙琳, 秦兴雷. 前白蛋白和N末端脑利钠肽前体对老年心力衰竭患者预后的影响[J]. 中华实用诊断与治疗杂志, 2015, 29(9): 848. -




 下载:
下载: