-
精神分裂症属于重性精神疾病,病人主要特征为认识(思维与感知)、行为活动异常。在人们生产生活方式不断改变的今天,精神分裂症临床发病率表现出逐年升高趋势。地卓西平(MK-801)可以通过拮抗N-甲基-D-天冬氨酸(NMDA)受体方式模拟精神分裂症病人阳性(快速移动)与阴性(包括刻板行为和焦虑情绪)症状[1-2]。临床常对精神分裂症采取利培酮进行治疗,尤其对于合并情感障碍病人,可产生良好的疗效[3]。当前,银杏叶提取物(extract of Ginkgo biloba,EGB)治疗精神分裂症相关研究很多,但涉及MK-801致精神分裂症模型大鼠实验的相关作用机制研究较少。鉴于此,本研究以上述模型大鼠为对象,研究给予EGB对该模型大鼠的改善作用及其机制,以期为EGB的进一步研发及临床应用提供实验依据。
-
40只Sprague-Dawley(SD)大鼠,且均为成年雄性,体质量为250~300 g,来自黑龙江中医药大学动物实验中心,许可证号:SCXK(黑)2013-004。置于20~26 ℃环境饲养,湿度控制为50%~60%,对其定期清洗消毒,饲养7 d后开始实验。
-
LC-6A型高效液相色谱仪,购自日本岛津公司;AG125型电子天平,购自梅特勒-托利多仪器(上海)有限公司;离心机(型号为TGL-16),购自上海医疗器械厂);WHI型漩涡震荡器,购自浙江乐成电器厂;TU-1900型双光束紫外线可见光光度计,购自北京普析通用仪器公司;Morris水迷宫与旷场实验相关测试系统,由上海欣软信息科技有限公司提供。
-
自行配置的0.9%氯化钠溶液;MK-801(美国SIGMA公司,临用时将其配制为0.01 mg/mL的注射液);EGB761(Beaufour Ipsen Industrie,临用时将其配制为100 mg/L的溶液);利培酮(齐鲁制药,国药准字:H20041807,临用时将其配制为0.036 mg/mL的混悬液);丙二醛(MDA)试剂盒(批号:A003)、超氧化物歧化酶(SOD)试剂盒(批号:A001-3),均购自南京建成生物工程研究所;自行配置的95%乙醇;谷氨酸(Glu)标准品,购自sigma公司;蒸馏水等。
-
将40只大鼠随机分为空白组、模型组、对照组与实验组,各10只。模型组、对照组与实验组大鼠采取腹腔注射方式注入0.01 mg/mL MK-801,取下侧腹腔较为靠近外侧1/3部位,连续注射2周;空白组大鼠连续注射2周0.9%氯化钠溶液,注射体积同其他3组。建模后,对照组大鼠每天使用0.05 mL/kg利培酮悬浮液进行灌胃治疗;实验组每天使用200 mg/kg EGB761进行灌胃治疗;另外2组使用等体积蒸馏水,连续2周。
-
Glu表达测定:采取HPLC-ECD法,在1 mL预冷95%乙醇之中加入大鼠额前脑组织,进行离心处理,取5 mg样品放入离心管,再添加衍生工作液50 μL,进行涡旋震荡处理1 min之后,取20 μL放进色谱仪,详细记录色谱图,最后计算峰面积,获取Glu表达情况。以黄嘌呤氧化酶法(WST-1)进行血清SOD水平的测定;以硫代巴比妥酸法(TBA)进行血清MDA水平的测定;均严格按照试剂盒说明书进行。
-
逃避潜伏期:灌胃治疗结束前5 d,把4组大鼠置于Morris水迷宫之中自由游泳1 min,让其熟悉环境,确保大鼠泳姿以及速度正常,在治疗结束前4、3、2、1、0 d(评估第1、第2、第3、第4、第5天)把4组大鼠置于Morris水迷宫之中训练,每只训练2组/天,1 min内没有找到平台表明逃逸潜伏期60 s,把各大鼠置于不同象限,注意放入时保证其面向水池壁,详细记录具体逃逸潜伏期。
-
旷场实验:完成逃避潜伏期检测后,采用旷场实验测试系统(组成包括分析软件、测验箱、视频图样采样卡以及视频合成器等)跟踪大鼠活动,记录其具体活动轨迹,并且算出活动路程;其中测验箱选择排净水Morris水迷宫,控制环境之内均照明200 lx,并且伴50 dB白噪音,把大鼠置于无安全平台相应无水水池之中,大鼠依然寻找安全平台,使其自由活动10 min,详细记录大鼠穿越次数、中央活动路程比(中心区活动路程/总路程)、中央活动时间比(中心区活动时间/总时间)。
-
采用t检验和q检验。
-
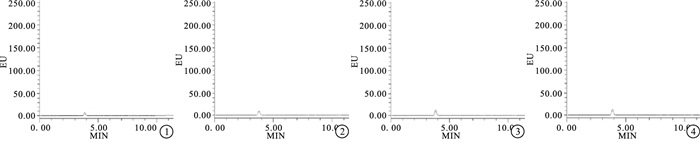
与空白组相比,模型组大鼠MDA水平明显升高,SOD、Glu表达水平明显降低,差异均有统计学意义(P < 0.05)。与模型组相比,对照组与实验组MDA水平明显降低,SOD、Glu表达水平明显升高,差异均有统计学意义(P < 0.01)。与对照组相比,实验组Glu表达水平明显升高,差异有统计学意义(P < 0.01),MDA、SOD水平差异无统计学意义(P>0.05)(见表 1)。各组大鼠脑组织Glu HPLC色谱图见图 1。
分组 n MDA/(nmol/mL) SOD/(U/mL) Glu/(ng/g) 空白组 10 4.22±0.45 258.12±27.36 6.82±0.73 模型组 10 11.90±1.23# 129.80±13.75# 4.15±0.52# 对照组 10 4.26±0.48** 241.24±25.36** 5.62±0.58** 实验组 10 4.23±0.45** 244.78±25.16** 6.84±0.75**△△ F — 273.37 64.11 38.10 P — < 0.01 < 0.01 < 0.01 MS组内 — 0.009 0.468 5.482 q检验:与空白组比较#P < 0.05;与模型组比较**P < 0.01;与对照组比较△△P < 0.01 表 1 各组大鼠血清MDA、SOD水平及脑组织Glu表达比较(x±s)
-
评估第1天、第2天,与空白组相比,模型组、对照组与实验组大鼠逃避潜伏期明显延长,差异均有统计学意义(P < 0.05),而模型组、对照组与实验组3组间比较差异无统计学意义(P>0.05)。评估第3天、第4天、第5天,与模型组相比,对照组与实验组大鼠逃避潜伏期明显缩短,差异均有统计学意义(P < 0.01),而对照组与实验组2组间比较差异无统计学意义(P>0.05)(见表 2)。
分组 n 第1天 第2天 第3天 第4天 第5天 空白组 10 45.31±5.02 45.26±4.98 45.23±4.94 45.52±4.93 45.48±4.90 模型组 10 54.36±5.98# 54.40±5.51# 54.37±5.52# 54.76±5.58# 54.73±5.64# 对照组 10 53.78±5.61# 50.72±5.68# 46.02±4.90** 45.17±4.65** 44.23±4.52** 实验组 10 53.52±5.59# 50.35±5.62# 45.98±4.88** 45.02±4.63** 44.15±4.50** F — 5.99 4.74 7.30 9.23 10.75 P — < 0.01 < 0.01 < 0.01 < 0.01 < 0.01 MS组内 — 10.179 12.368 3.216 5.069 1.478 q检验:与空白组比较#P < 0.05;与模型组比较**P < 0.01 表 2 各组大鼠Morris水迷宫逃避潜伏期比较(x±s;s)
-
与空白组相比,模型组大鼠穿越次数、中央活动时间比与中央活动路程比均明显增加,差异有统计学意义(P < 0.05)。与模型组相比,对照组与实验组穿越次数、中央活动时间比与中央活动路程比均明显增加,差异有统计学意义(P < 0.01),对照组与实验组2间比较差异均无统计学意义(P>0.05)(见表 3)。
分组 n 穿越次数 中央活动时间比 中央活动路程比 空白组 10 2.62±0.28 67.25±6.94 66.97±7.02 模型组 10 0.65±0.07# 24.12±2.83# 24.36±3.25# 对照组 10 2.43±0.28** 51.76±5.38** 50.13±5.89** 实验组 10 2.56±0.30** 52.65±5.41** 51.98±5.94** F — 142.42 113.42 96.40 P — < 0.01 < 0.01 < 0.01 MS组内 — 4.376 2.058 5.473 q检验:与空白组比较#P < 0.05;与模型组比较**P < 0.01 表 3 各组大鼠旷场实验行为比较(x±s)
-
MK-801能够通过抑制神经冲动与人脑中兴奋传导通路,阻碍神经兴奋传导,最终引起神经递质传递障碍。同时,MK-801也能有效阻断颞叶-海马系统与额叶-海马系统NMDA受体,导致海马神经细胞功能出现缺陷。因而,实验常采用MK-801建立精神分裂症动物模型。有研究[4]表明,随EGB761剂量增加,表现出剂量依赖关系,高剂量症状改善效果更好。故本研究直接选择200 mg·kg-1·d-1 EGB761,未根据剂量分组进行研究。
SOD清除氧自由基主要通过催化超氧阴离子O2-生成过氧化氢H2O2方式,再由过氧化氢酶(CAT)与谷胱甘肽过氧化物酶(GSH-Px)催化H2O2形成具有安全无害性产物[水(H2O)与氧(O2)],同时SOD亦能保护CAT以及GSH-Px不被O2-灭活,防止脂质过氧化反应损伤细胞。相关研究[5]表明,精神分裂症病人会产生血清抗氧化物质水平异常现象,推测脑内存在大量氧自由基,同时生理性清除功能减弱,使得脂质过氧化反应损伤加重,对病人中枢神经系统发挥毒性作用,可能促进精神分裂症发生及发展。MDA属于机体内氧自由基在抗氧化物质参与链式反应下形成的降解产物,可一定程度反映精神分裂症病人体内脂质过氧化程度,如果氧自由基堆积量增多,则会加剧脂质过氧化,由此会生成大量MDA。氧化-抗氧化系统动态平衡被破坏,将出现氧化应激反应,损伤脑组织之中神经细胞,引起精神分裂症等各种精神障碍疾病,而SOD和MDA表达与氧化应激反应损伤具有相关性。有研究指出,Glu系统活动异常,可对神经元可塑性产生影响,引起神经毒性,同时启动神经元分泌Glu等递质,对γ-氨基丁酸能神经元上相应NMDA受体产生作用,从而形成负反馈作用来调节Glu释放水平;MK-801可以破坏该循环回路里面的NMDA受体,引起兴奋性传导处于脱抑制状态,导致脑内递质失衡,最终引发精神症状[6-7]。相关研究[8-9]发现,EGB能够起到保护Glu导致的兴奋性毒性损害的功效。EGB治疗精神分裂症主要伦理依据为:发挥抗氧化以及质膜稳定功能,EGB可优化中枢神经能力代谢状态,减少自由基,有效降低脂质过氧化反应,达到改善脑血液流变性目的[10-11]。本实验中,与空白组相比,模型组大鼠MDA水平明显升高,SOD、Glu表达水平明显降低;与模型组相比,对照组与实验组MDA水平明显降低,SOD、Glu表达水平明显升高;与对照组相比,实验组Glu表达水平明显升高。提示大鼠模型存在血清MDA水平显著升高、血清SOD水平与脑组织Glu表达显著降低的现象,而EGB能够促进血清MDA、SOD水平和脑组织Glu表达恢复,产生良好的抗氧化与抑制脂质过氧化的功效。
Morris水迷宫可用于评估大鼠空间认知功能与记忆学习能力[12]。旷场实验能够评估情绪反应情况、中枢兴奋状态、自主探索活动能力以及运动功能等,通常中央区域探索活动量降低,说明中枢兴奋性减弱,出现情绪障碍(如抑郁)行为;如果周边区域自主活动逐渐增多,则表示兴奋性升高且出现焦虑恐惧情绪[13-14]。同时,旷场实验也能在一定程度上将模型大鼠记忆能力有效反映出来。本实验结果显示,评估第1天、第2天,与空白组相比,其余3组逃避潜伏期具有明显延长表现,且3组间比较无统计学意义;评估第3天、第4天、第5天,与模型组相比,对照组与实验组大鼠逃避潜伏期明显缩短;与空白组相比,模型组大鼠平均穿越次数、中央活动时间比以及中央活动路程比明显更大;与模型组相比,对照组与实验组平均穿越次数、中央活动时间比与中央活动路程比明显增加,与蔡菡等[15]研究结论一致。说明EGB能够提高精神分裂症大鼠认知与学习记忆能力,改善不良情绪。
综上所述,EGB对MK-801致精神分裂症模型大鼠的改善作用机制可能为通过抑制脂质过氧化反应,改善Glu功能障碍引起的精神分裂症状,从而提高记忆、认知能力,缓解不良情绪状态。但本次实验样本较少,且未比较不同剂量与不同时间处理结果,具有一定局限性,更详细、确切的作用机制仍待后续更全面、更大样本的研究进一步证实。
银杏叶提取物对地卓西平致精神分裂症模型大鼠的改善作用及其机制研究
Improvement effects of the extract of Ginkgo biloba on the schizophrenia model rats induced by dizocilpine and its mechanism
-
摘要:
目的探讨银杏叶提取物(extract of Ginkgo biloba,EGB)对地卓西平(MK-801)致精神分裂症模型大鼠的改善作用及其机制。 方法选择40只清洁级雄性Sprague-Dawley(SD)成年大鼠,将其随机分为空白组、模型组、对照组与实验组,各10只,空白组腹腔注射0.9%氯化钠溶液,模型组、对照组与实验组均腹腔注射MK-801,对照组加用利培酮,实验组加用EGB,比较4组血清丙二醛(MDA)与超氧化物歧化酶(SOD)水平、额前脑组织谷氨酸(Glu)表达情况、各时间逃避潜伏期、旷场实验指标。 结果与空白组相比,模型组大鼠MDA水平明显升高,SOD、Glu表达水平明显降低,差异均有统计学意义(P < 0.05)。与模型组相比,对照组与实验组MDA水平明显降低,SOD、Glu表达水平明显升高,差异均有统计学意义(P < 0.01)。与对照组相比,实验组Glu表达水平明显升高,差异有统计学意义(P < 0.01)。评估第1天、第2天,与空白组相比,模型组、对照组与实验组大鼠逃避潜伏期均明显延长,差异有统计学意义(P < 0.05)。评估第3天、第4天、第5天,与模型组相比,对照组与实验组大鼠逃避潜伏期均明显缩短,差异有统计学意义(P < 0.01)。与空白组相比,模型组大鼠穿越次数、中央活动时间比与中央活动路程比均明显增加,差异有统计学意义(P < 0.05)。与模型组相比,对照组与实验组穿越次数、中央活动时间比与中央活动路程比均明显增加,差异有统计学意义(P < 0.01)。 结论EGB能有效改善MK-801致精神分裂症,促进神经认知功能恢复,减少焦虑、恐惧情绪,与其降低MDA、SOD水平,发挥抑制脂质过氧化作用,纠正Glu功能障碍相关。 Abstract:ObjectiveTo analyze the improvement effects of extract of Ginkgo biloba(EGB) on the schizophrenia model rats induced by dizocilpine(MK-801), and its mechanism. MethodsForty clean male Sprague-Dawley(SD) adult rats were randomly divided into the blank group, model group, control group and experimental group(10 rats in each group). The blank group was intraperitoneally injected with 0.9% sodium chloride solution. The model group, control group and experimental group were intraperitoneally injected with MK-801. The control group was additionally injected with risperidone, while the experimental group was additionally treated with EGB. The serum levels of malondialdehyde(MDA) and superoxide dismutase(SOD), expression of glutamate(Glu) in frontal brain tissues, escape latency time and open field test parameters were compared among four groups. ResultsCompared with the blank group, the MDA level was significantly higher, and the expression levels of SOD and Glu were significantly lower in model group(P < 0.05). Compared with the model group, the level of MDA was significantly lower, and the expression levels of SOD and Glu were significantly higher in the control group and experimental group(P < 0.01). Compared with the control group, the expression level of Glu was significantly higher in the experimental group(P < 0.01). On the first and second day of evaluation, the escape latency in model group, control group and experimental group were significantly longer than that in blank group(P < 0.05). On the third, fourth and fifth day of evaluation, the escape latency in control group and experimental group were significantly shorter than that in model group(P < 0.01). Compared with the blank group, the crossing frequency, central activity time ratio and central activity distance ratio in the model group significantly increased(P < 0.05). Compared with the model group, the crossing frequency, central activity time ratio and central activity distance ratio in the control group and experimental group significantly increased, and the differences of which were statistically significant(P < 0.01). ConclusionsEGB can effectively relieve the schizophrenia caused by MK-801, promote the recovery of neurocognitive function, and decrease anxiety and fear, which is related to the reduction of MDA and SOD levels, inhibition of lipid peroxidation and correction of Glu dysfunction. -
Key words:
- schizophrenia /
- extract of Ginkgo biloba /
- dizocilpine /
- rat
-
表 1 各组大鼠血清MDA、SOD水平及脑组织Glu表达比较(x±s)
分组 n MDA/(nmol/mL) SOD/(U/mL) Glu/(ng/g) 空白组 10 4.22±0.45 258.12±27.36 6.82±0.73 模型组 10 11.90±1.23# 129.80±13.75# 4.15±0.52# 对照组 10 4.26±0.48** 241.24±25.36** 5.62±0.58** 实验组 10 4.23±0.45** 244.78±25.16** 6.84±0.75**△△ F — 273.37 64.11 38.10 P — < 0.01 < 0.01 < 0.01 MS组内 — 0.009 0.468 5.482 q检验:与空白组比较#P < 0.05;与模型组比较**P < 0.01;与对照组比较△△P < 0.01 表 2 各组大鼠Morris水迷宫逃避潜伏期比较(x±s;s)
分组 n 第1天 第2天 第3天 第4天 第5天 空白组 10 45.31±5.02 45.26±4.98 45.23±4.94 45.52±4.93 45.48±4.90 模型组 10 54.36±5.98# 54.40±5.51# 54.37±5.52# 54.76±5.58# 54.73±5.64# 对照组 10 53.78±5.61# 50.72±5.68# 46.02±4.90** 45.17±4.65** 44.23±4.52** 实验组 10 53.52±5.59# 50.35±5.62# 45.98±4.88** 45.02±4.63** 44.15±4.50** F — 5.99 4.74 7.30 9.23 10.75 P — < 0.01 < 0.01 < 0.01 < 0.01 < 0.01 MS组内 — 10.179 12.368 3.216 5.069 1.478 q检验:与空白组比较#P < 0.05;与模型组比较**P < 0.01 表 3 各组大鼠旷场实验行为比较(x±s)
分组 n 穿越次数 中央活动时间比 中央活动路程比 空白组 10 2.62±0.28 67.25±6.94 66.97±7.02 模型组 10 0.65±0.07# 24.12±2.83# 24.36±3.25# 对照组 10 2.43±0.28** 51.76±5.38** 50.13±5.89** 实验组 10 2.56±0.30** 52.65±5.41** 51.98±5.94** F — 142.42 113.42 96.40 P — < 0.01 < 0.01 < 0.01 MS组内 — 4.376 2.058 5.473 q检验:与空白组比较#P < 0.05;与模型组比较**P < 0.01 -
[1] 陈溪, 谷洪顺, 张兰, 等. 淫羊藿苷对MK-801致精神分裂症小鼠模型的影响[J]. 中国康复理论与实践, 2016, 22(4): 395. doi: 10.3969/j.issn.1006-9771.2016.04.005 [2] 赵永厚, 赵玉萍, 高潇, 等. 愈癫汤对MK-801致精神分裂症模型大鼠NO信号通路的影响[J]. 中华中医药杂志, 2017, 32(11): 5081. [3] 周本宏, 张红盼, 郭敏, 等. 补肾壮阳胶囊对小鼠认知功能障碍的改善作用及机制研究[J]. 中国医院药学杂志, 2016, 36(20): 1739. [4] THANCHAROEN O, LIMWATTANANON C, WALEEKHACHONLOET O, et al. Ginkgo biloba extract(EGb761), cholinesterase inhibitors, and memantine for the treatment of mild-to-moderate alzheimer's disease: a network meta-analysis[J]. Drugs Aging, 2019, 36(5): 435. doi: 10.1007/s40266-019-00648-x [5] 李金凤, 徐桂梅, 张辰子, 等. 银杏叶提取物对MPTP诱导帕金森小鼠保护作用的研究[J]. 中国比较医学杂志, 2016, 26(1): 46. [6] 白钰, 吕全胜, 马晓丽. 银杏叶提取物对PC12细胞损伤的保护作用[J]. 中国临床药理学杂志, 2016, 32(16): 1495. [7] 徐芳, 刘红梅, 黄莺. 银杏叶提取物对特发性肺间质纤维化成纤维细胞表型转化过程中NOTCH信号通路的影响[J]. 中国中西医结合急救杂志, 2016, 23(4): 417. doi: 10.3969/j.issn.1008-9691.2016.04.019 [8] 潘秀娟, 刘家洪. 银杏叶联合齐拉西酮治疗慢性精神分裂症的有效性及安全性研究[J]. 辽宁中医杂志, 2015, 42(7): 1262. [9] 李新纯, 李庆, 王超英, 等. 银杏叶胶囊联合阿立哌唑对精神分裂症患者认知功能的影响[J]. 中医杂志, 2016, 57(18): 1583. [10] 房茂胜, 钱红, 曾宽, 等. ω-3PUFAs对精神分裂症模型大鼠认知功能的影响[J]. 中华行为医学与脑科学杂志, 2017, 26(7): 589. [11] 张潇剑, 张姣, 韩怀钦, 等. GAD67-GFP精神分裂症小鼠行为学改变及海马齿状回颗粒细胞层GABA能神经元的表达[J]. 神经解剖学杂志, 2015, 31(3): 332. [12] 欧阳俊摇, 邹海艳, 于萍, 等. 银杏叶提取物对慢性脑缺血模型大鼠脑组织突触后致密物-95蛋白及递质氨基酸的影响[J]. 国际中医中药杂志, 2016, 38(4): 336. [13] 张昊, 印海翔, 徐颺, 等. MK-801诱导精神分裂症小鼠的c-Fos及NADPH氧化酶通路机制研究[J]. 现代生物医学进展, 2015, 15(22): 4252. [14] 王巍, 张昊, 徐颺, 等. 帕潘立酮治疗MK-801诱导精神分裂症小鼠的效果分析及PI3K/Akt/mTOR信号通路蛋白的参与作用[J]. 中南药学, 2017, 15(7): 911. [15] 蔡菡, 程万良, 徐磊. MK-801建立精神分裂症动物模型研究进展[J]. 精神医学杂志, 2015, 28(3): 235. -





 下载:
下载: