-
精神分裂症是一种病因不明,且病人的临床表现、治疗反应及病程都不相同的疾病,临床表现主要为思维、情感、认知和行为方面的异常[1-2]。病人及家属的生活质量都会受到很大的影响,大部分病人需要长期服用抗精神病药物来控制临床症状[3]。世界范围内超过2万人受到精神分裂症的困扰,其主要发病于成年早期,中国民众的终身患病率已经超过1%[4-5]。利培酮(RIS)是国内最早上市的非典型抗精神病药物,临床应用广泛[6-7]。其在肝内主要经细胞色素P450(CYP2D6)代谢为9-羟基利培酮(9-OHRIS),9-OHRIS与RIS有同样的药理作用[8-9]。但近年来国内外研究[10-11]表明RIS可能会影响病人的甲状腺功能指标。甲状腺激素为人体正常生长发育所必需,其分泌不足或过量都可引起疾病。本研究建立了RIS临床血药浓度测定的方法,并回顾性选取单独服用RIS的116例病人的临床资料,分析RIS血药浓度与甲状腺功能指标的相关性,为临床合理制定RIS用药方案提供参考。
-
超高效液相色谱仪(ACQUITY UPLC-Class,美国Waters);三重四级杆质谱仪(XEVO TQ-S,美国Waters);JW-2017HR型高速冷冻离心机(安徽嘉文仪器装备有限公司公司);XW-80A型旋涡混合器(上海青浦沪西仪器厂);奥豪斯CP214分析天平(美国奥豪斯公司);C8000型生化分析仪(美国雅培公司);Milli-Q Biocel超纯水仪(美国Millipore公司)。
-
RIS购于中国药品生物制品检定所,含量>98%,9-OHRIS购于美国sigma公司,含量>99%,乙腈为色谱级(美国TEDIA公司),乙酸铵为色谱级(美国sigma公司),氨水为色谱纯(上海阿拉丁试剂有限公司),四甲基乙二胺(美国sigma公司),水为超纯水,其余试剂均为分析纯。
-
选取2022年1-8月收治的精神分裂症住院病人116例。纳入标准:(1)符合国际疾病分类第十版(ICD-10)中的精神分裂症诊断标准;(2)年龄18~60岁;(3)阳性与阴性症状量表(PANSS)总分≥60分;(4)住院6周以上;(5)使用RIS片(商品名:维思通,生产企业:西安杨森制药有限公司)治疗,未合用其他抗精神病药物。排除标准:(1)合并其他基础疾病如高血压、糖尿病等;(2)甲状腺功能亢进或减退;(3)妊娠与哺乳期孕妇;(4)有药物滥用史。
-
收集实验室信息系统(LIS)中病人RIS血药浓度检测结果,并通过电子病历系统查阅病人性别、年龄、身高、体质量及RIS日剂量等相关资料。本次研究样本数据均为RIS给药4~5 d后稳态血药浓度。病人于住院第2、4、6周早晨服药前采集静脉血3 mL。离心后取血清在2~8 ℃保存,并进行生化指标检测,包括三碘甲状腺原氨酸(T3)、四碘甲状腺原氨酸(T4)、游离三碘甲状腺素(FT3)、游离甲状腺素(FT4)和促甲状腺激素(TSH)等。
-
BEH C18(50×2.1 mm)色谱柱,流动相为乙腈-水(A,含10 mmol/L乙酸铵溶液和0.01%氨水),梯度洗脱(梯度设置为0~1.5 min,40%~95%乙腈; 1.5~2.0 min,65%~95%乙腈; 2.0~2.1 min,95%~40%乙腈; 2.1~2.5.5 min,40%~40%乙腈),流速0.5 mL/min,柱温40 ℃,进样量2 μL。
-
离子源:电喷雾离子源。电离模式:正离子模式,毛细管电压为3.0 kV,源温度150 ℃,脱溶剂温度550 ℃,氮气脱溶气流量1 000 L/h,氮气锥气流量为150 L/h。操作模式:多反应监测(MRM)模式,化合物的电离模式、母离子、子离子、锥孔电压(cone voltage,CV)和碰撞能量(collision energy,CE)。具体见表 1。
药物 母离子 子离子 CV/V CE/eV RIS 411.14 191.10 10 18 9-OHRIS 427.27 207.15 30 28 表 1 分析物的母离子、子离子、CV值和CE值
-
标准品溶液:精密称取20.00 mg的RIS标准品粉末,用适量甲醇溶解与稀释得质量浓度为2.0 μg/mL的工作液。精密称量10.00 mg的9-OHRIS标准品粉末,用适量乙腈溶解与稀释配制质量浓度为2.0 μg/mL的工作液。
内标(IS)溶液:精密称取20.00 mg的氯米帕明标准品粉末,用甲醇与乙腈稀释得质量浓度为0.8 μg/mL的内标工作液。所有溶液储存于4 ℃冰箱。样本处理:取200 μL含药血清于1.5 mL于EP管中,再加入20 μL内标,混匀后加入600 μL乙腈,充分涡旋混匀1 min,离心6 min(4 ℃,16 000 r/min),取上清液,即得含药血清供试品。空白血清的处理方法同前,即得空白血清供试品。
-
分别取空白血清、空白血清加入药物以及病人服药后的血清样品,采用1.6项下处理方法处理,并进样分析。
-
取一定体积的RIS、9-OHRIS加入到空白血清中,分别配制成质量浓度为0.4~120 ng/mL的血清标准品,余下操作按1.6项下方法处理。进样分析,记录色谱图。以待测物质量浓度(X)为横坐标、待测物与内标峰面积的比值(Y)为纵坐标,制备标准曲线。
-
按照1.6中的方法配制RIS、9-OHRIS质量浓度为1.0、30.0和100.0 ng/mL的含药血清,每个浓度平行6份,分3批按“1.6”项下方法操作,在不同工作日测定,计算平均值、日内、日间精密度与准确度。
-
取空白血清,分别精密加入不同体积的RIS、9-OHRIS对照品工作液,配制成RIS、9-OHRIS质量浓度为1.0和100.0 ng/mL的含药血清,并分别置于常温下储存4 h和24 h、2~8 ℃冰箱冷藏48 h、-20 ℃冷冻30 d和冻融3个循环后,按1.6项下的方法进行处理并分析,求出相对标准差(relative standard deviation,RSD)。
-
取空白血清,分别精密加入不同体积的RIS、9-OHRIS对照品工作液,配制成RIS、9-OHRIS质量浓度为1.0、30.0、100.0 ng/mL的含药血清,再各加入20 μL的内标溶液,处理后进样分析,记录峰面积为A。另将空白血清用乙腈沉淀后加入对照品工作液,配制成同样的质控浓度,不经过提取过程,按上述同样方法测定各峰面积,记录为B。以乙腈代替空白血清配制同样质控浓度的RIS、9-OHRIS,取2 μL,注入液质联用仪测定,各色谱峰面积记录为C。提取回收率(%)=A/B×100%,基质效应(%)=B/C×100%。
-
按照1.6中的方法配制成RIS、9-OHRIS质量浓度为100.0 ng/mL的含药血清,按照血清样品的处理分析方法进行处理分析;再取空白血清供试品注入液质联用仪测定。对峰面积进行比较,查看是否有残留效应。
-
采用单因素方差分析和Pearson相关分析。
-
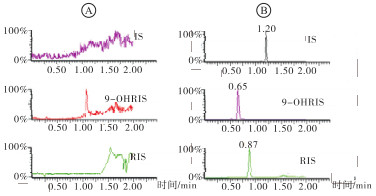
空白血清中的内源性物质不干扰RIS、9-OHRIS和内标(IS)的测定,其保留时间分别在0.65、0.87、1.09、2.0 min左右(见图 1)。
-
实验结果表明血清中RIS和9-OHRIS在0.4~120.0 ng/mL内线性关系良好,具有代表性的线性回归方程为:$\stackrel{\wedge}{Y}=0.0396X+0.0100$,R2= 0.995(RIS);$\stackrel{\wedge}{Y}=0.0292X+0.00736$,R2=0.994(9-OHRIS)。
-
RIS、9-OHRIS在血清中的3个质控浓度的精密度和准确度实验结果显示,所有的RSD值均 < 10.29%,RIS、9-OHRIS的日内准确度和日间准确度均能满足生物样品定量原则(中国药典通则9012)规定的变异系数不超过15%的要求(见表 2)。
分析物 药物量/(ng/mL) 日内 日间 测定值(x±s)/(ng/mL) RSD/% 准确度/% 测定值(x±s)/(ng/mL) RSD/% 准确度/% RIS 1.00 1.03 ±0.09 9.18 103.17 1.00±0.10 10.29 100.04 9-OHRIS 30.00 30.15±0.92 3.06 100.49 29.12±1.84 6.32 97.05 100.00 96.35±5.67 5.88 96.35 92.77±5.11 5.50 92.77 1.00 0.97±0.05 4.94 96.50 1.00±0.09 9.34 99.72 30.00 29.41±0.92 3.11 98.02 27.50±1.53 5.58 91.68 100.00 95.68±2.70 2.82 95.68 92.92±4.49 4.83 92.92 表 2 RIS、9-OHRIS在人血清中的日内、日间准确度和精密度(ni=6)
-
含低浓度和高浓度的RIS、9-OHRIS血清在常温下4 h和24 h、2~8 ℃冰箱冷藏48 h、长期冷冻条件下以及反复冻融循环条件下稳定性良好,准确度范围在86.06%~110.83%之间,满足生物样品定量原则(中国药典通则9012)规定的平均准确度在±15%范围内的要求(见表 3)。
分析物 储存条件 添加药物量/(ng/mL) 测定值(x±s)/(ng/mL) 准确度/% RIS -20 ℃下3次冻融循环 1.00 0.99±0.06 100.02 100.00 98.34±3.37 98.34 冷冻30 d (-20 ℃) 1.00 0.98±0.07 98.33 100.00 92.08±2.33 92.08 室温4 h 1.00 1.07±0.05 107.17 100.00 92.43±3.11 室温24 h 1.00 0.92±0.11 91.50 100.00 92.43±3.11 92.43 2~8 ℃48 h 1.00 1.11±0.03 110.83 100.00 95.14±0.04 95.14 9-OHRIS -20 ℃下3次冻融循环 1.00 1.04±0.04 107.45 100.00 98.74±1.81 98.74 冷冻30 d (-20 ℃) 1.00 1.04±0.04 103.83 100.00 95.68±2.70 95.68 室温4 h 1.00 1.11±0.04 107.17 100.00 86.06±0.78 86.06 室温24 h 1.00 1.06±0.02 106.00 100.00 86.61±0.98 86.61 2~8 ℃48 h 1.00 1.08±0.03 108.33 100.00 97.28±3.06 97.28 表 3 RIS、9-OHRIS在人血清中的稳定性试验结果(ni=6)
-
结果显示,RIS、9-OHRIS低、中、高3个浓度的提取回收率与基质效应能满足生物样品定量原则(中国药典通则9012)规定的变异系数不超过15%的要求。内标氯米帕明的提取回收率为(96.93±1.85)%,基质效应为(97.20±3.21)%(见表 4)。
分析物 药物量/(ng/mL) 基质效应/% 提取回收率/% RIS 1.00 96.32 ±6.41 96.99 ±3.93 9-OHRIS 30.00 94.38±3.15 98.95±8.09 100.00 94.81±7.72 96.30±6.54 1.00 87.20±1.77 87.47±6.28 30.00 88.29±3.29 94.83±3.49 100.00 87.12±1.02 97.80±6.54 表 4 RIS、9-OHRIS的提取回收率和基质效应结果(ni=6)
-
在连续进3针高浓度样品后,进样的空白血清图谱在4.09、2.05 min处没有明显的残留峰。
-
本研究纳入病人共116例,其中男83例,女33例;年龄19~60岁;体质量40~105 kg;体质量指数(BMI)16~37 kg/m2;RIS日剂量2~6 mg;住院时间4~8周。病人的稳态谷质量浓度为16.33~116.73 ng/mL,平均质量浓度为(49.76±18.07)ng/mL。
-
对48例病人的指标Pearson相关性分析结果显示,RIS血药浓度与BMI指数、年龄、性别相关性均无统计学意义(r=-0.124、-0.04、0.178,P>0.05)。
-
治疗各时间点病人的稳态血药浓度差异无统计学意义(P>0.05),甲状腺功能指标除TSH外(P>0.05),其他4个指标治疗后随着时间的推移呈波动上升趋势(P < 0.01)(见表 5)。
时间点 RIS血药质量浓度/(ng/mL) T3 T4 TSH FT3 FT4 治疗前 0 1.60±0.35 85.47±40.59 2.96±2.40 4.69±0.81 12.75±5.28 第2周 48.68±21.42 1.53±0.36 70.44±44.67 3.02±2.23 4.43±0.89 10.50±6.16 第4周 49.73±19.76 1.66±0.34 83.53±35.31 3.14±2.75 4.80±0.80 13.06±5.10 第6周 50.86±21.69 1.70±0.37 90.77±32.83 3.15±2.99 4.90±0.80 13.63±4.47 F 0.31 5.05 5.80 0.15 6.97 7.82 P >0.05 <0.01 <0.01 >0.05 <0.01 <0.01 MS组内 439.910 0.126 1491.890 6.809 0.682 27.954 表 5 治疗各时间点RIS血药浓度与甲状腺功能指标的比较(n=116;x±s)
-
随机取第4周数据进行相关性分析显示,总体分析时RIS血药浓度与甲状腺功能指标均无相关性(P>0.05),分性别分析发现男性病人无明显相关性,但女性病人的RIS血药浓度与T4、FT3、FT4水平呈正相关(P < 0.05)(见表 6)。
性别 n T3 T4 TSH FT3 FT4 不区分 116 0.080 0.166 -0.088 0.073 0.125 男性 83 -0.058 0.029 -0.002 -0.128 -0.028 女性 33 0.434 0.480* -0.342 0.524* 0.454* *P<0.05 表 6 RIS血药浓度与甲状腺功能的Pearson相关性分析(r)
-
相较于既往利用高效液相色谱-串联质谱法(HPLC-MS/MS)测定RIS血药浓度的方法[12],本研究应用UPLC-MS/MS技术建立的测定方法,该法具有操作简便、检测灵敏度高、特异性强和分析效率高等特点,且在进样量(1~2 μL vs.5~10 μL)和分析时间方面均具有一定优势。
RIS是一种新型的非典型抗精神病药物,与其他传统抗精神病药物比较,其很大的优势就是不良反应较小,因此临床使用非常广泛。但近年来已经有研究报道了其可能增加精神分裂症病人甲状腺功能异常的风险[10, 13],因此关注RIS血药浓度与甲状腺功能指标的相关性具有重要意义。李宝琴等[14]研究发现RIS单药治疗后,FT3和TT4的血清水平降低,与治疗前相比差异有统计学意义; 而FT4、TT3及TSH水平与治疗前相比,差异无统计学意义。而吴会清等[15]发现FT3、FT4及TT3的血清水平下降,TSH血清水平升高,与治疗前相比差异有统计学意义。但沈家民[16]通过对临床数据的分析并未发现RIS会影响甲状腺指标。但目前的研究多未分性别进行分析,且大部分的研究主要聚焦于给药前后,并未研究血药浓度与甲状腺指标的相关性,因此在本研究中,笔者尝试对不同性别的病人进行分析,结果表明虽然在给药前后甲状腺功能指标并无显著性差异,且总体分析中RIS血药浓度与甲状腺功能指标也无相关性。但分性别研究后我们发现女性病人的血药浓度与T4、FT3、FT4都显著相关,T3与TSH的相关性虽然没有显著性但P值接近0.05,可能是因为此次研究的统计样本较小。男性病人的RIS血药浓度与甲状腺功能指标则依然无相关性。这种性别差异的产生可能是由于RIS会影响女性的雌激素代谢系统[17],而受影响的雌激素代谢机制进一步影响了甲状腺功能,而RIS血药浓度影响女性病人甲状腺功能的具体机制还有待于进一步研究。这些结果提示我们在临床使用RIS时应重点关注女性病人的甲状腺功能指标,对女性病人进行血药浓度监测是必要的。本研究虽然在一定程度上说明了一些问题,但仍存在一定的局限性。首先,因为在临床中精神病病人单用RIS的病例较少,导致本研究的样本量相对较小。第二,受限于精神病病人的特殊性,研究中的受试者均来自本地区的精神病专科医院,其他普通医院病例较少,未收集到多中心的数据。第三,目前的研究结果只能初步说明女性甲状腺功能指标与RIS血药浓度之间的关系,更深层次的机制与原因有待于在后续的基础研究中进一步探究。
综上所述,RIS是一种新型的非典型抗精神病药物,与其他传统抗精神病药物相比,其不良反应明显减少,但其依旧有可能增加精神分裂症病人甲状腺功能紊乱的风险[18-19]。基于此,本研究建立了一种基于UPLC-MS/MS的RIS血药浓度快速测定方法,并用于临床中的血药浓度监测。此外本研究发现RIS引起甲状腺功能紊乱的风险与性别有很大的相关性,因此关注女性病人RIS血药浓度对甲状腺功能的影响具有重要意义。我们需要密切关注病人RIS血药浓度的变化,提高RIS疗效的同时有效避免相关不良反应的发生,推动临床合理化用药。
利培酮血药浓度与甲状腺功能的相关性研究
Study on the correlation between blood concentration of risperidone and thyroid function indexes
-
摘要:
目的建立利培酮(RIS)血药浓度测定方法,探讨RIS治疗精神分裂症病人的血药浓度与甲状腺功能指标的相关性。 方法血浆样品经乙腈沉淀后,以氯米帕明为内标,采用超高效液相色谱-串联质谱(UPLC-MS/MS)法测定,色谱柱为BEH C18,流动相为乙腈-水(含5 mmol/L乙酸铵溶液和0.01%氨水),梯度洗脱,流速为0.5 mL/min,柱温为40 ℃,进样量为2 μL,采用多反应监测模式扫描,对UPLC-MS/MS进行方法学考察,将其用于测定116例临床精神分裂症病人血浆中RIS浓度,收集相关病例的住院信息,并探讨RIS血药浓度与甲状腺功能指标的相关性。 结果RIS、9-羟基利培酮(9-OHRIS)在0.4~120.0 ng/mL范围内线性关系良好;日内、日间准确度、提取回收率、基质效应及稳定性均符合要求。病人体内平均稳态血药质量浓度为(49.76±18.07)ng/mL;治疗各时间点病人的稳态血药浓度差异无统计学意义(P>0.05),甲状腺功能指标除促甲状腺激素外(P>0.05),其他4个指标治疗后随着时间的推移呈波动上升趋势(P < 0.01);病人的血药浓度与甲状腺功能指标无相关性(P>0.05),但女性病人的RIS血药浓度与四碘甲状腺原氨酸、游离三碘甲状腺素、游离甲状腺素均呈正相关(r=0.480、0.524、0.454,P < 0.05)。 结论该方法准确简便、快速灵敏、重现性好,可用于测定精神分裂症病人体内RIS的血药浓度。女性病人体内较高的血药浓度可能会影响甲状腺功能指标,进而影响病人甲状腺功能,需要引起临床的注意。 Abstract:ObjectiveTo establish a method for the determination of blood concentration of risperidone (RIS), and to explore the correlation between blood concentration of RIS and thyroid function indexes in patients with schizophrenia. MethodsThe plasma samples were precipitated with acetonitrile, and then determined by ultra performance liquid chromatography-tandem mass spectrometry (UPLC-MS/MS) with clomipramine as the internal standard.The chromatographic column was BEH C18, and the mobile phase was acetonitrile-water (containing 5 mmol/L ammonium acetate solution and 0.01% ammonia) with gradient elution.The flow rate was 0.5 mL/min, the column temperature was 40 ℃, and the injection volume was 2 μL.The methodology of UPLC-MS/MS was investigated by multiple reaction monitoring scanning, and it was used to determine the plasma RIS concentration in 116 patients with schizophrenia.The hospitalization information of related cases was collected, and the correlation between RIS blood concentration and thyroid function indexes was explored. ResultsRIS and 9-OHRIS had a good linear relationship in the concentration range of 0.4-120.0 ng/mL.The intra-day and inter-day accuracy, extraction recovery, matrix effect and stability met the requirements.The mean steady-state plasma concentration was (49.76±18.07)ng/mL.There was no significant difference in the steady-state plasma concentration of patients at each time point of treatment (P>0.05).Except for TSH (P>0.05), the other four indicators showed a fluctuating upward trend over time after treatment (P < 0.05), but the RIS plasma concentration of female patients was positively correlated with T4, FT3 and FT4 (r=0.480, 0.524, 0.454, P < 0.05). ConclusionsThe method is accurate, simple, rapid, sensitive and reproducible, and can be used to determine the plasma concentration of RIS in patients with schizophrenia.Higher blood drug concentration in female patients may affect the thyroid function index, and then affect the thyroid function of patients, which needs clinical attention. -
Key words:
- schizophrenia /
- risperidone /
- plasma concentration /
- thyroid function
-
表 1 分析物的母离子、子离子、CV值和CE值
药物 母离子 子离子 CV/V CE/eV RIS 411.14 191.10 10 18 9-OHRIS 427.27 207.15 30 28 表 2 RIS、9-OHRIS在人血清中的日内、日间准确度和精密度(ni=6)
分析物 药物量/(ng/mL) 日内 日间 测定值(x±s)/(ng/mL) RSD/% 准确度/% 测定值(x±s)/(ng/mL) RSD/% 准确度/% RIS 1.00 1.03 ±0.09 9.18 103.17 1.00±0.10 10.29 100.04 9-OHRIS 30.00 30.15±0.92 3.06 100.49 29.12±1.84 6.32 97.05 100.00 96.35±5.67 5.88 96.35 92.77±5.11 5.50 92.77 1.00 0.97±0.05 4.94 96.50 1.00±0.09 9.34 99.72 30.00 29.41±0.92 3.11 98.02 27.50±1.53 5.58 91.68 100.00 95.68±2.70 2.82 95.68 92.92±4.49 4.83 92.92 表 3 RIS、9-OHRIS在人血清中的稳定性试验结果(ni=6)
分析物 储存条件 添加药物量/(ng/mL) 测定值(x±s)/(ng/mL) 准确度/% RIS -20 ℃下3次冻融循环 1.00 0.99±0.06 100.02 100.00 98.34±3.37 98.34 冷冻30 d (-20 ℃) 1.00 0.98±0.07 98.33 100.00 92.08±2.33 92.08 室温4 h 1.00 1.07±0.05 107.17 100.00 92.43±3.11 室温24 h 1.00 0.92±0.11 91.50 100.00 92.43±3.11 92.43 2~8 ℃48 h 1.00 1.11±0.03 110.83 100.00 95.14±0.04 95.14 9-OHRIS -20 ℃下3次冻融循环 1.00 1.04±0.04 107.45 100.00 98.74±1.81 98.74 冷冻30 d (-20 ℃) 1.00 1.04±0.04 103.83 100.00 95.68±2.70 95.68 室温4 h 1.00 1.11±0.04 107.17 100.00 86.06±0.78 86.06 室温24 h 1.00 1.06±0.02 106.00 100.00 86.61±0.98 86.61 2~8 ℃48 h 1.00 1.08±0.03 108.33 100.00 97.28±3.06 97.28 表 4 RIS、9-OHRIS的提取回收率和基质效应结果(ni=6)
分析物 药物量/(ng/mL) 基质效应/% 提取回收率/% RIS 1.00 96.32 ±6.41 96.99 ±3.93 9-OHRIS 30.00 94.38±3.15 98.95±8.09 100.00 94.81±7.72 96.30±6.54 1.00 87.20±1.77 87.47±6.28 30.00 88.29±3.29 94.83±3.49 100.00 87.12±1.02 97.80±6.54 表 5 治疗各时间点RIS血药浓度与甲状腺功能指标的比较(n=116;x±s)
时间点 RIS血药质量浓度/(ng/mL) T3 T4 TSH FT3 FT4 治疗前 0 1.60±0.35 85.47±40.59 2.96±2.40 4.69±0.81 12.75±5.28 第2周 48.68±21.42 1.53±0.36 70.44±44.67 3.02±2.23 4.43±0.89 10.50±6.16 第4周 49.73±19.76 1.66±0.34 83.53±35.31 3.14±2.75 4.80±0.80 13.06±5.10 第6周 50.86±21.69 1.70±0.37 90.77±32.83 3.15±2.99 4.90±0.80 13.63±4.47 F 0.31 5.05 5.80 0.15 6.97 7.82 P >0.05 <0.01 <0.01 >0.05 <0.01 <0.01 MS组内 439.910 0.126 1491.890 6.809 0.682 27.954 表 6 RIS血药浓度与甲状腺功能的Pearson相关性分析(r)
性别 n T3 T4 TSH FT3 FT4 不区分 116 0.080 0.166 -0.088 0.073 0.125 男性 83 -0.058 0.029 -0.002 -0.128 -0.028 女性 33 0.434 0.480* -0.342 0.524* 0.454* *P<0.05 -
[1] JAUHAR S, JOHNSTONE M, MCKENNA PJ. Schizophrenia[J]. Lancet, 2022(10323): 399. [2] MCCUTCHEON RA, MARQUES TR, HOWES OD. Schizophrenia-An Overview[J]. JAMA Psychiatry, 2020, 77(2): 201. doi: 10.1001/jamapsychiatry.2019.3360 [3] ROBINSON DG, SCHOOLER NR, PATRICIA M, et al. Outcomes during and after early intervention services for first-episode psychosis: results over 5 years from the RAISE-ETP Site-Randomized Trial[J]. Schizophr Bull, 2022, 48(5): 1021. doi: 10.1093/schbul/sbac053 [4] HUANG Y, WANG Y, WANG H, et al. Prevalence of mental disorders in China: a cross-sectional epidemiological study[J]. Lancet Psychiatry, 2019, 6(3): 211. doi: 10.1016/S2215-0366(18)30511-X [5] BAXTER AJ, CHARLSON FJ, CHENG HG, et al. Prevalence of mental, neurological, and substance use disorders in China and India: a systematic analysis[J]. Lancet Psychiatry, 2016, 3(9): 832. doi: 10.1016/S2215-0366(16)30139-0 [6] 陈寿林, 龚坚, 甄茂全. 小剂量利培酮治疗首发精神分裂症的疗效及安全性分析[J]. 中国卫生检验杂志, 2022, 32(3): 331. [7] 罗骞, 占海燕, 廖丹. 利培酮药物不良反应/事件277例临床特点分析[J]. 药品评价, 2022, 19(11): 692. [8] ALLADI CG, MOHAN A, SHEWADE DG, et al. Risperidone-induced adverse drug reactions and role of DRD2 and 5HTR2C genetic polymer-phisms in patients with schizophrenia[J]. J Pharmaol Pharmacother, 2017, 8(1): 28. doi: 10.4103/jpp.JPP_197_16 [9] 赵明坤, 刘叶红, 张平, 等. 利培酮对精神分裂症患者血脂和甲状腺激素的影响[J]. 中国临床药理学杂志, 2015, 31(187): 342. [10] 张嘉萱, 邓顺顺, 邱玛丽, 等. 利培酮单药或联合用药治疗后甲状腺激素水平的变化[J]. 中国临床药理学与治疗学, 2020, 25(10): 1145. [11] VEDAL TSJ, STEEN NE, BIRKELAND KI, et al. Free thyroxine and thyroid-stimulating hormone in severe mental disorders: a naturalistic study with focus on antipsychotic medication[J]. J Psychiatr Res, 2018, 106: 74. doi: 10.1016/j.jpsychires.2018.09.014 [12] 何秀玲, 谭金华, 宋天云, 等. HPLC-MS/MS法同时测定人血浆中利培酮和帕利哌酮的浓度[J]. 中南药学, 2021, 19(6): 1161. [13] 寇泽刚. 阿立哌唑、喹硫平和利培酮对精神分裂症患者甲状腺素水平的影响[J]. 蚌埠医学院学报, 2015, 40(9): 1184. doi: 10.13898/j.cnki.issn.1000-2200.2015.09.013 [14] 李宝琴, 秦青, 赵景, 等. 利培酮对精神分裂症患者甲状腺激素、细胞间黏附因子-1的影响[J]. 哈尔滨医科大学学报, 2013, 47(3): 250. [15] 吴会清, 杨梅, 盛利. 利培酮对精神分裂症患者血糖、血脂代谢指标及甲状腺激素水平的影响[J]. 河北医药, 2017, 39(20): 3068. [16] 沈家民. 利培酮与阿立哌唑对精神分裂症患者甲功五项的影响比较[J]. 当代医学, 2019, 25(25): 88. [17] 李红丽, 王高华, 王晓萍, 等. 利培酮对女性精神分裂症患者血清催乳素和雌二醇的影响[J]. 武汉大学学报(医学版), 2008, 29(6): 807. -





 下载:
下载: